Estrojenler
İnsan vücudunda doğal olarak bulunan birincil biyoeşdeğer (bioidentical) form olan estradiol, transfeminenler için uygulanan HRT’de kullanılan temel estrojendir. Estradiol hemihidrat (EH), özünde estradiol ile eşdeğer ve birbirinin yerine kullanılabilen başka bir estradiol formudur. Ayrıca bazen estradiol yerine estradiol esterleri (örn. estradiol valerat) de kullanılmaktadır. Estradiol esterleri, estradiolün ön ilaçları (vücutta estradiol’e dönüşmektedirler) ve biyolojik etkileri estradiol ile temelde aynıdır. Ancak enjeksiyon yoluyla kullanıldıklarında enjeksiyon bölgesinden daha yavaş emildikleri için daha uzun etki süreleri vardır ve bu; daha uzun aralıklarla doz alımı imkanı sağlamaktadır. Başlıca estradiol esterleri olarak estradiol valerat (EV), estradiol sipionat (EC), estradiol enantat (EEn), estradiol undesilat (EU) ve poliestradiol fosfat (PEP) örnek gösterilebilir.
- Estradiol valerat (EV), Türkiye’de piyasada yalnızca tablet formunda bulunmaktadır (Cyclo-Progynova, Climen, Divina), yurt dışında ise piyasada enjeksiyon formlarında da bulunmaktadır (Progynon Depot, Delestrogen).
- Estradiol sipionat (EC), yurt dışında enjeksiyon formunda bulunmaktadır (Depo-Estradiol).
- Estradiol enantat (EEn), yurt dışındaki resmi piyasada transfeminenler için kullanılması önerilmeyen bir progestin ile kombine şeklinde bulunmaktadır buna karşın yurt dışında bulunan bazı yerel eczane ve/veya ilaç firmaları tarafından üretilmektedirler.
- Estradiol undesilat (EU), piyasadan çekilmiştir ve resmi olarak piyasada bulunmamaktadır fakat yurt dışında bulunan yerel eczane ve/veya ilaç firmaları tarafından üretilmektedirler.
- Poliestradiol fosfat (PEP), polimer biçimindeki enjekte edilebilir bir estradiol ön ilacıdır; yavaş metabolize olur ve çok uzun etki süresine sahiptir. Resmi piyasada geçtiğimiz yıllarda bulmak gittikçe zorlaşmıştır ya da bazı ülkelerde piyasadan tamamen çekilmiştir (Estradurin).
Biyoeşdeğer olmayan estrojenler örneğin etinilestradiol (EE; doğum kontrol haplarında bulunur), konjuge estrojenler (CEEs; piyasa ismi Premarin; menopoz hormon tedavisinde kullanılır) ve dietilstilbestrol (DES; eskiden yaygın olarak kullanılmakta olup günümüzde kullanılmamaktadır), karaciğer metabolizmasına daha dirençlidir ve estradiol gibi biyoeşdeğer estrojenlerle karşılaştırıldığında (Aly, 2020) karaciğerde estrojen aracılı sentez üzerinde orantısız etkiler göstermektedirler. Bu sebeple pıhtılaşma üzerinde çok daha güçlü bir etkiye sahiptirler ve kan pıhtısı ile ilişkili kardiyovasküler sorunlar gibi belirli sağlık problemleri açısından daha yüksek risk taşımaktadırlar (Aly, 2020). Aynı zamanda testosteron baskılanması için çok daha yüksek dozlara ihtiyaç duyulabilmesi nedeniyle de, biyoeşdeğer olmayan estrojenler transfeminenlerin HRT’sinde ideal olarak asla kullanılmamalıdır. Bunlara örnek olarak piyasada Diane, Drospera, Desolett, Myralon, Ginera, Reginon, Dienille, Crogynon, Ranova, Leverette, Yasmin, Elleacnelle, Gynelle, Drosetil isimleri ile bulunurlar.
Estradiol, testislere sahip bireylerde (AMAB) doz ile bağlantılı bir şekilde testosteron seviyelerini baskılamaktadır. Fizyolojik ve kılavuz temelli estradiol seviyeleri (<200 pg/mL veya <734 pmol/L), gonadları alınmamış (Slack et al., 2023; Krishnamurthy et al., 2023; Liang et al., 2018) transfeminenlerde testosteron seviyelerini cis kadın aralığına düşürmek için genellikle yeterli olmamaktadır. Bu nedenle transfeminenler HRT’de iken estradiol genellikle antiandrojen veya progestojen ile birlikte kullanılmaktadır (Hembree et al., 2017; Rose et al., 2021; Coleman et al., 2022). Bu kombinasyonda estradiol, testosteron seviyelerini kısmen baskılarken, geriye kalan testosteron da antiandrojen veya progestojen tarafından ek olarak baskılanmaktadır. Her ne kadar kombinasyon içeren HRT’nin testosteronu tam olarak baskılamada veya engellemede etkili olabilse de (örn. CPA veya bikalutamid ile), bazı antiandrojen ve progestojen türleriyle testosteron baskılanmasının eksik kalabildiği durumlar da mevcuttur (örn. spironolakton) (Jain et al., 2019). Buna karşın fizyolojik estradiol seviyeleriyle kıyaslandığında, fizyolojik üstü (veya sürafizyolojik: cis kadın değerlerinin üstü) estradiol seviyeleri tek başına estradiol kullanımıyla testosteron seviyelerini düzenli ve tam biçimde cis kadın aralığına kadar baskılayabilmektedir (Gooren et al., 1984 [Grafik]; Igo & Visram, 2021; Herndon et al., 2023). Bu alternatif yaklaşım sıklıkla yüksek doz estradiol monoterapisi olarak adlandırılmaktadır ve antiandrojenler ile progestojenlerin yan etkilerinden, risklerinden ve maliyetlerinden kaçınma avantajına sahiptir. Ancak bu yaklaşım uluslararası rehberlerin önerdiği seviyelerin üzerine çıkan estradiol seviyeleri ile tek başına estradiolün sebep olduğu daha yüksek sağlık riskleri dezavantajını da taşır. Klinik uygulamada sıklıkla fizyolojik estradiol dozları ve kombinasyon içeren HRT tercih edilirken, yüksek doz estradiol monoterapisi genellikle (dışarıdan yardım almadan) kendi kendine (DIY) HRT uygulayan transfeminenlerde daha sık görülmektedir.
Estradiolün feminenleştirici etkilerinin, androjen yokluğunda ve nispeten düşük seviyelerde maksimize olduğu görülmektedir. Daha yüksek estradiol dozları ve fizyolojik üstü estradiol seviyeleri, testosteronun daha fazla baskılanmasını sağlama dışında, transfeminenlerde daha iyi bir feminenleşme ile ilişkili değildir (Deutsch, 2016; Nolan & Cheung, 2021). Her ne kadar aksi düşünülse de yapılan çalışmalardan elde edilen bazı veriler, HRT’nin erken dönemlerinde uygulanan yüksek estrojen dozlarının, meme gelişimini olumsuz etkileyebileceğine işaret etmektedir. Bu sebeple transfeminenlerin HRT’sindeki asıl hedef, belli bir estradiol seviyesine ulaşmaktan ziyade testosteron seviyelerinin baskılanması üzerinedir. Yüksek estrojen dozlarının (bu örnekte estradiol dahil) kan pıhtısı ve kardiyovasküler sorunlar gibi istenmeyen sağlık etkileri açısından riskleri de daha yüksektir (Aly, 2020). Dolayısıyla transfeminenler için fizyolojik estradiol dozlarının kullanımı idealdir. Bununla birlikte yetersiz testosteron baskılanması durumunda yüksek estrojen dozları daha faydalı olabilmektedir, oral yol olmayan diğer yollardan alınan biyoeşdeğer estradiol söz konusu olduğunda mutlak risk çok daha düşüktür; bu durum daha çok belli başlı risk faktörlerine (örn. ileri yaş, fiziksel hareketsizlik, obezite, eşzamanlı progestojen kullanımı, sigara kullanımı, cerrahi işlemler, nadir trombofilik bozukluklar) sahip kişilerde ciddi önem taşımaktadır. Daha fazla/yeterli testosteron baskılanması gerekiyorsa, ilgili risk faktörleri taşımayan (örn. sağlıklı genç bireyler) kişilerde, sınırlı derecede fizyoloji-üstü dozlarda oral yol ile olmayan estradiol kullanımı, risk-yarar dengesi açısından makul olabilmektedir (Aly, 2020).
Estradiol ve estradiol esterleri transfeminenlerin HRT’sinde genellikle oral yol ile (ağızdan), dil altından (sublingual), transdermal (cilde uygulanarak), enjeksiyon ile (intramüsküler veya subkütan) veya implant şeklinde kullanılmaktadır (Wiki).
Oral Estradiol
Transfeminenlerin HRT’sinde estradiol, ağız yoluyla(tablet formunda) kullanılmaktadır (Wiki; Grafikler). Alternatif olarak bazı ülkelerde, örneğin birçok Avrupa ülkesinde, ağızdan estradiol valerat (EV) tabletleri de kullanılmaktadır. Bu iki estradiol şekli arasındaki tek fark, estradiol valeratın (EV) ester bileşeni nedeniyle ağırlık olarak biraz daha az estradiol (~%76) içermesidir ve bu sebeple eşdeğer estradiol düzeyleri için biraz daha yüksek dozlara (~1.3 kat) ihtiyaç duymasıdır (Wiki; Tablo).
| *Türkiye’de piyasada bulunan Estrofem ve Trisequens (mavi ve kırmızı tabletleri) estradiol hemihidrat içermektedir. Piyasa isimleri olan Climen, Cyclo-Progynova ve Divina her biri beyaz tabletlerinde (bahsedilen üç ilaç kutusunun içerisinde beyaz renkli olmayan diğer tabletler kombine tabletlerdir ve genellikle kullanılmaları önerilmemektedir) estradiol valerat içermektedir. |
Oral estradiol günde tek doz için uygun bir etki süresine sahip olmakla birlikte kullanımı çok pratik ve ucuz olduğu için transfeminenlerde en popüler ve eyaygın kullanılan estradiol biçimidir. Oral estradiol göreceli olarak %5 gibi düşük bir biyo-yararlanım(uygulanan ilaç miktarının dolaşıma geçen oranı) seviyesine sahiptir ve aynı dozla elde edilen estradiol düzeylerinde kişiler arasında önemli farklılıklar görülmektedir. Dolayısıyla bazı transfeminenlerde, oral estradiol ile yeterli estradiol düzeyleri oluşmayabilir ve bu durum kullanılan anti-androjene de bağlı olarak testosteron baskılanmasının yetersiz kalmasına neden olabilmektedir.
Oral estradiolün temel dezavantajı, ilk geçiş etkisi nedeniyle karaciğerde aşırı estradiol seviyeleri oluşturması ve estrojenle modüle edilen karaciğer sentezinde orantısız bir etki yaratmasıdır (Aly, 2020). Bu da pıhtılaşmayı arttırarak kan pıhtıları ve kardiyovasküler sorunlar gibi ilgili sağlık komplikasyonları riskini yükseltmektedir (Aly, 2020). Bu dezavantajlar estradiol yeterli ve aşırı olmayan dozlarda oral olmayan yollardan alındığında büyük ölçüde ortadan kalkmaktadır. Bu sebeple transdermal estradiol gibi oral olmayan estradiol formları, oral kullanım kadar pratik olmamakla birlikte daha büyük ekonomik maliyetleri olmasına rağmen transfeminenlerin HRT’sinde daha çok tercih edilmektedir. Yaşla birlikte artan kan pıhtısı ve kardiyovasküler problemlerin riski nedeniyle, 40 ve 45 yaş üstü tüm transfeminenlerin oral olmayan yollardan estradiol kullanmaları önerilmektedir (Aly, 2020; Coleman et al., 2022). Yüksek doz estradiol monoterapisi için gereken yüksek estradiol seviyeleri ve oral olmayan formlar ile kıyasla daha fazla riskleri nedeniyle, oral estradiol transfeminenler için yüksek doz estradiol monoterapisinde iyi bir tercih değildir. Karaciğere orantısız etkisinin yanı sıra, oral estradiol; oral olmayan formlarla kıyaslandığında estron (E1) ve estron sülfat (E1S) gibi fizyolojik olmayan düzeylerde estradiol metabolitlerine yol açmaktadır. Bu durumun varsa da klinik sonuçları bilinmemektedir. Yinede mevcut çalışmalar oral ve oral olmayan fomlarda estradiolün transfeminenlerde feminenleşme ve meme gelişimi açısından benzer etkililiğe sahi olduğunu göstermektedir (Sam, 2020).
Dil Altı (sublingual) Estradiol
Oral estradiol tabletleri, ağız yoluyla yutulmak yerine dil altından(sublingual) alınabilmektedir. Dil altından alınan estradiol tabletlerinin biyo-yararlanım seviyesi, oral uygulamayla karşılaştırıldığında birkaç kat daha yüksektir ve dolayısıyla kanda ölçülen estradiol seviyeleri önemli ölçüde daha yüksek çıkmaktaktadır (Sam, 2021; Wiki; Grafikler). Oral uygulama yerine dil altı estradiol kullanımı, dozların ve dolayısıyla ilaçların kişide yarattığı ekonomik baskının azaltılmasına ve gerek duyulduğunda testosteron seviyelerinin baskılanmasını iyileştirmek amacıyla tercih edilebilmektedir.
Bununla birlikte dil altı estradiol, oral estradiole kıyasla estradiol seviyelerinde çok belirgin piklere neden olur ve yüksek estradiol düzeylerinin kısa süreli devam etmesiyle sonuçlanmaktadır. Bu nedenle dil altı estradiolün gün boyunca bölünmüş dozlar(örn. günde üç kere –8 saatte bir–) halinde alınarak estradiol seviyelerinin daha sabit tutulması önerilmektedir. Transfeminenlerde bu piklere sahip seviyelerin sonuçları (örn. testosteron baskılanması ve sağlıkları riskleri açısından) çok az araştırılmıştır ve büyük ölçüde bilinmemektedir. Buna rağmen günde birkaç kez alınarak yüksek doz estradiol monoterapisi şeklinde kullanıldığında güçlü fakat hala tam olarak yeterli olmayan testosteron baskılanması gözlemlenmiştir (Yaish et al., 2023). Oral estradiol valerat tabletleri de benzer şekilde oral yol yerine dil altında tutulabilir ve bu şekilde kullanıldıklarında aynı derecede etkili oldukları görülmüştür (Aly, 2019; Wiki). Tabletlerin dil altı alınılmaya çalışıldığı durumlarda tabletlerin bir kısmının istemsiz bir şekilde yutulması nedeniyle, dil altı estradiol uygulaması pratikte hem dil altı hem de kısmen oral uygulamanın bir karşımı olabilmektedir ve oral estradiole benzer sağlık risklerine bir ölçüde sahip olabilmektedir (Wiki). Estradiolün bukkal(yanak içi) uygulanması, dil altı uygulamayla benzer özelliklere sahip görünmektedir ancak bu konuda çok daha az araştırma vardır ve transfeminenlerde yaygın olarak kullanılmamaktadır (Wiki).
Transdermal Estradiol
Transdermal estradiol, bant (yama da denmektedir), jel, emülsiyon ve sprey formlarında mevcuttur (Wiki). Bu formlar genellikle kol, karın veya kalça gibi cilt bölgelerine uygulanmaktadır. Jel, emülsiyon ve spreyler uygulandıktan sonra kısa bir süre kuruması beklenir; bantlar ise belirli bir süre boyunca ciltte yapışık kalmaktadır. Cilt yoluyla emilim hızının sınırlı olması (rate-limited absorption) nedeniyle, transdermal estradiolde bir depo etkisi oluşur ve estradiol düzeyleri uzun süre boyunca sabit kalmaktadır. Bu nedenle estradiol jel, emülsiyon ve spreyleri günde bir yada birkaç kez kullanım için uygundur. Bantlar marka/ürün tipine bağlı olarak 3—4 veya 7 gün boyunca ciltte kalarak devamlı estradiol salınımı sağlar (Tablo). Transdermal estradiol, oral estradiole göre daha pahalıdır. Jel, emülsiyon ve spreyler oral uygulamaya göre daha az pratik bulunabilir ancak bantlar seyrek uygulanmaları nedeniyle kişiye daha kolay gelebilmektedir. Öte yandan bantlar bazen uygulandığı bölgede kızarıklı ve tahriş gibi sorunlara yol açabilir veya banttaki yapıştırıcının erken gevşemesi sonucu düşebilmektedir. Oral estradiolde olduğu gibi transdermal estradiolde de estradiol düzeylerinde önemli bireysel farklılıklar görülmektedir; bazı transfeminenlerde emilim düşük kalabilmekte olup düşük estradiol düzeylerine ve yetersiz testosteron baskılanmasına neden olabilmektedir. Örneğin Türkiye’de piyasada bulunmayan ve ismi Lenzetto olan estradiol spreyleri gibi estradiol spreyleri transfeminenler için yeterli etkiyi sağlayamayan çok düşük estradiol seviyeleri verdiği için önerilmemektedir (Aly, 2020; Grafik).
40 yaş üstü transfeminenlerde, oral estradiole kıyasla daha düşük sağlık riskleri nedeniyle genellikle transdermal estradiol tercih edilmektedir. Testosteron baskılanması için gereken yüksek estradiol seviyelerine ulaşmak zor olduğundan, transdermal estradiol jelleri yüksek doz estradiol monoterapisi için uygun bir seçenek değildir. Öte yandan birden fazla estradiol bandın (örn. 100 μg/gün sağlayan bantlar; örn. Climara Forte [Türkiye’de piyasada bulunmaktadır]) aynı anda kullanılması yüksek doz estradiol monoterapisinde etkili olabilmektedir; ancak bu birçok bandın aynı anda kullanılmasıyla yüksek maliyetlere sebep olabilmektedir (Wiki).
Farklı cilt bölgeleri, transdermal estradiolü farklı oranlarda emmektedir (Wiki). Özellikle genital bölgeye (skrotum veya neovajina) uygulama, klasik cilt bölgelerinde kıyasla çok daha yüksek estradiol emilimi sağlayabilir ve bu da standart uygulamaya göre çok daha yüksek estradiol düzeyleriyle sonuçlanabilmektedir (Aly, 2019). Bu tarz bir yaklaşım, doz ve dolayısıyla ilaç maliyetini azaltmak veya daha iyi testosteron baskılanması için gerek duyulduğunda daha yüksek estradiol seviyelerine ulaşmak amacıyla yararlı olabilmektedir. Estradiolün memelere uygulanması ise meme gelişimini iyileştirdiğine veya hızlandırdığında dair bir kanıt olmadığı ve potansiyel sonuçları (örn. meme kanseri riski) nedeniyle önerilmemektedir.
Enjeksiyon Estradiol
Enjeksiyon halindaki estradiol preparatları, kas içine (intramüsküler; IM) veya deri altına (subkütan; SC; SubQ) uygulanabilmektedir (Wiki; Wiki; Grafikler). Estradiol esterlerinin enjeksiyonunda bir tür -depo- etkisi oluşur; bu sayede enjeksiyon bölgesinden yavaşça emilirler ve uzayan bir etki süresine sahip olurlar. Etki süresi kullanılan estere bağlı olarak birkaç günden birkaç hafta hatta aylara kadar değişebilmektedir. Kısa ve orta etki süreli yaygın kullanılan enjekte edilebilir estradiol esterleri arasında estradiol valerat (EV), estradiol sipionat (EC), estradiol enantat (EEn) ve estradiol benzoat (EB) bulunmaktadır. Daha uzun etki süresine sahip estradiol esterleri (örn. estradiol undesilat [EU] ve poliestradiol fosfat [PEP]) ise artık ilaç firmaları tarafından üretilmemekte olup temin edilememektedir. Kas içi (IM) enjeksiyon durumunda genellikle deltoid kası (üst kol), vastus lateralis ve rektus femoris kasları (uyluk) veya ventrogluteal kas (kalça) enjeksiyon bölgeleri olarak kullanılmaktadır. Deri altı yağ içi (SubQ) daha az yaygın olmakla birlikte intramüsküler (IM) enjeksiyonla benzer farmakokinetik özellikler göstermektedir ve uygulaması daha kolay, daha az ağrılı ve daha pratiktir (Wiki). Ancak subkütan (SubQ) yolla güvenli ve rahat bir şekilde enjekte edilebilecek maksimum hacim, intramüsküler (IM) enjeksiyona kıyasla daha düşüktür (uygulama bölgesine bağlı olarak 1.5—3 mL ve 2—5 mL’ye kadar) (Hopkins, & Arias, 2013; Usach et al., 2019). Enjeksiyon formundaki estradiol genellikle daha ucuz olma eğilimindedir, ancak düzenli enjeksiyon gerektirdiğinden diğer uygulama yollarına kıyasla daha az kullanışlı olabilmektedir. Uzun vadede, enjeksiyon bölgesinde iç skar dokusu (iz dokusu) oluşma riski de söz konusu olabilmektedir. Estradiol enjeksiyonları dünyanın birçok yerinde (örn. Türkiye dahil olmak üzere Avrupa’nın büyük kısmında) piyasadan çekilmiştir ve bu ilaçlara erişim oldukça sınırlıdır. Son yıllarda birçok transfeminen bu uygulama yolunu kullanmak amacıyla resmi olmayan biçimlerde (yerel eczane ve/veya ilaç firmaları tarafından satılan; “homebrew” diye tabir edilen ve karaborsa piyasasında resmi olmayan bir biçimde satılan) hazırlanmış enjekte edilebilir estradiol preparatlarına yönelmektedirler.
Enjekte edilebilir estradiol preparatları genellikle diğer estradiol formlarına göre daha yüksek dozlarda kullanılır ve çok daha yüksek estradiol düzeylerine kolaylıkla ulaşabilmektedir. Bu durum testosteron baskılanması için yararlı olabilmektedir, ve dolayısıyla; enjeksiyon formundaki estradiolün, transfeminenlerde yüksek doz estradiol monoterapisi açısından en iyi seçenek olduğunu varsaymak pek mümkündür. Bunlarla birlikte enjeksiyon formundaki estradiol preparatlarıyla mümkün olan bu yüksek dozlar kolaylıkla aşırı doz kullanımına ve gereksiz yere artan risklere yol açabilmektedir (Aly, 2020).Ne yazık ki bu konuyla ilgili mevcut sağlık kılavuzlarının önerdiği enjeksiyon formundaki estradiol ester dozları ve aralıkları, aşırı yüksek ve çok seyrek uygulanır görünmektedir (örn. 10—40 mg/2 hafta, estradiol valerat[EV]); bu da kişinin HRT’den istediği sonucu alamamasıyla birlikte kişinin sağlık durumu açısından pek uygun olmayabilmektedir (Aly, 2021).
Yaklaşık 300 pg/mL (1.100 pmol/L) ortalama estradiol seviyesi hedefiyle yüksek doz estradiol monoterapisi için önerilen enjeksiyon estradiol ester dozları ve aralıkları aşağıda gösterilmiştir:
(Hedeflenen estradiol düzeyi yaklaşık 300 pg/mL [1.100 pmol/L])
| Estradiol Esteri | Kısa Aralık | Orta Aralık | Uzun Aralık | Simülasyon: |
| Estradiol benzoat (EB) | 0,67 mg/1 gün | 1,33 mg/2 gün | 2 mg/3 gün | [Grafik] |
| Estradiol valerat (EV) | 2 mg/3 gün | 3,5 mg/5 gün | 5 mg/7 gün | [Grafik] |
| Estradiol sipionat (EC) (yağ içinde) | 5 mg/7 gün | 7 mg/10 gün | 10 mg/14 gün | [Grafik] |
| Estradiol sipionat (EC) (süsp.) | 2 mg/3 gün | 3,5 mg/5 gün | 5 mg/7 gün | [Grafik] |
| Estradiol enantat (EEn) | 5 mg/7 gün | 7 mg/10 gün | 10 mg/14 gün | [Grafik] |
| Estradiol undesilat (EU)a | 10 mg/14 gün | 20 mg/28 gün | 30 mg/42 gün | [Grafik] |
| Poliestradiol fosfat (PEP) | 160 mg/30 gün | 240 mg/45 gün | 320 mg/60 gün | [Grafik] |
a Estradiol undecylate için dozlar ve aralıklar çıkarımsal ve varsayımsaldır (Aly, 2021).
Bu dozlar ve aralıklar bir başlangıç noktası olarak değerlendirilmeli; kan tahlilleri temelinde gerektiği şekilde düzenlenmesi gerekmekmektedir (bkz. HRT’nin takibi ve izlenmesi) . Eğer estradiol seviyeleri çok düşükse ve testosteron baskılanması yetersiz kalınıyorsa dozlar arttırılmalıdır; eğer estradiol seviyeleri çok yüksekse fakat testosteron baskılanması sağlanmışsa doz azaltılmalıdır. Eğer kişinin HRT rejimine bir antiandrojen veya progestojen eklenecekse, bunlar testosteron baskılanmasına yardımcı olacağından hedeflenen estradiol seviyesini 100–200 pg/mL (367–734 pmol/L) aralığında tutmak için dozların daha düşük olması gerekmektedir. Benzer şekilde, gonadları cerrahi yolla alınmış kişilerde testosteron baskılanması gerekmeyeceği için estradiol dozları daha düşük tutulmalıdır.
Estradiol İmplantları
Estradiol implantları, saf kristal hormon şeklindeki küçük implantlardır ve doktorlar tarafından cerrahi bir işlemle deri altındaki yağ dokusuna yerleştirilir (Wiki). Vücut tarafından emilimleri yavaşça gerçekleşir ve yeni implantlar 4 ila 6 ayda bir yerleştirilir. Küçük bir cerrahi işleme ihtiyaç duyulması, yüksek maliyet ve sınırlı bulunabilirlik/erişilebilirlik nedeniyle estradiol implantları, diğer estradiol uygulama yolları kadar sık kullanılmaz. Ayrıca dünyadaki hemen hemen tüm farmasötik estradiol implantları piyasadan çekilmiş durumdadır ve mevcut implantlar neredeyse yalnızca yerel eczanelerde hazırlanan ürünlerdir (compunding). Estradiol implantlarıyla doz ayarlaması da diğer uygulama yollarına göre daha zordur. Buna rağmen, estradiol implantları çok istikrarlı ve sabit estradiol seviyeleri sağlamaktadır ve çok uzun etki süreleri sayesinde mevcut estradiol formları arasında nispeten benzersiz bir kullanım kolaylığı sunmaktadır.
Ek Notlar
Yetişkina Transfeminenler için Estradiolün Mevcut Formları ve Önerilen Dozları*
| İlaç | Uygulama Yolu | Form | Doz |
| Estradiol | Oral | Tablet | 2–8 mg/gün |
| Dil altı veya bukkal | Tablet | 0.5–6 mg/günb | |
| Transdermal | Bant (yama) | 50–400 μg/gün | |
| Transdermal | Jel | 1.5–6 mg/gün | |
| Transdermal | Sprey | Önerilmemektedirc | |
| Subkütan implant | Pellet | 25–150 mg/6 ay | |
| Estradiol valerat (EV) | Oral | Tablet | 3–10 mg/günd |
| Dil altı veya bukkal | Tablet | 1–8 mg/günb,d | |
| IM veya SubQ enjeksiyon | Yağ solüsyonu | 0.75–4 mg/5 gün; veya 1–6 mg/7 gün; veya 1.5–9 mg/10 gün |
|
| Estradiol sipionat (EC) | IM veya SubQ enjeksiyon | Yağ solüsyonu | 1–6 mg/7 gün; veya 1.5–9 mg/10 gün; veya 2–12 mg/14 gün |
| Süspansiyon | 0.75–4 mg/5 gün; veya 1–6 mg/7 gün; veya 1.5–9 mg/10 gün |
||
| Estradiol enantat (EEn) | IM veya SubQ enjeksiyon | Yağ solüsyonu | 1–6 mg/7 gün; veya 1.5–9 mg/10 gün; veya 2–12 mg/14 gün |
| Estradiol benzoat (EB) | IM veya SubQ enjeksiyon | Yağ solüsyonu | 0.15–0.75 mg/gün; veya 0.3–1.5 mg/2 gün; veya 0.45–2.25 mg/3 gün |
| Estradiol undesilat (EU)e | IM veya SubQ enjeksiyon | Yağ solüsyonu | 2–12 mg/14 gün; veya 4–24 mg/28 gün; veya 6–36 mg/42 gün |
| Poliestradiol fosfat (PEP) | IM enjeksiyon | Solüsyon | 40–160 mg/ayf |
a Ergenlik (pubertal) dönemindeki transfeminenlerde, normal kadın ergenlik dönemini taklit etmek için daha düşük estradiol dozları kullanılmalıdır (Aly, 2020).
b Günde bir kez yerine, günde 2–4 kez (her 6–12 saatte bir) bölünmüş dozların kullanımı önerilmektedir (Sam, 2021).
c Bu estradiol formu, istenenden daha düşük estradiol seviyelerine neden olmasından dolayı önerilmemektedir. (Aly, 2020; Grafik).
d Estradiol valerat, estradiolün içerdiği miktarın yaklaşık %75’ini barındırdığı için aynı düzeyde estradiol elde etmek adına dozların estradiole göre yaklaşık ~1.3 kat daha fazla olması gerekmektedir (Aly, 2019; Sam, 2021).
e Estradiol undecylate’ın dozları ve enjeksiyon aralıkları, çıkarımsal ve varsayımsaldır (Aly, 2021).
f Daha yüksek bir yükleme (loading) dozu —örneğin, ilk bir veya iki enjeksiyon için 240 mg ya da 320 mg poliestradiol fosfat — estradiol seviyelerinin kararlı ve sabit hale (steady-state) daha hızlı ulaşmasını sağlayabilmektedir. Bununla birlikte, bu preparat yakın zamanda üretimden çekilmiştir ve piyasada artık bulunmamaktadır.
Estradiolün farklı formları, uygulama yolları ve dozları ile elde edilen estradiol seviyeleri (Wiki; Tablo) ve yaklaşık eşdeğer dozlarla ilgili ek kaynaklar da mevcuttur (Aly, 2020).
Kişiler arasında HRT sırasında elde edilen estradiol seviyelerinde çok büyük bir değişkenlik söz konusudur, aynı doz estradiol uygulamasında bile estradiol seviyeleri bireyler arasında önemli ölçüde farklı olabilmektedir. Bu değişkenlik oral ve transdermal estradiolde en yüksektir; ancak enjeksiyon formundaki estradiol preparatları ve diğer estradiol formlarında da kayda değer düzeydedir. Bu nedenle estradiol dozları mutlak olmamakla birlikte kan tahlilleriyle kılavuzluk edilerek kişiye özel düzenlenmelidir (bkz. HRT’nin takibi ve izlenmesi). Ayrıca bazı uygulama yollarında estradiol seviyelerinde dalgalanmalar (ve pikler) olabileceği için kan testleri arasında da ciddi farklar görülebilmektedir. Bu durum en belirgin şekilde dil altı (sublingual) estradiol ve enjeksiyon formundaki estradiol için geçerlidir. Bu uygulama yollarındaki dalgalanmalar (ve pikler) öngörülebilir olup, kan tahlili sonuçlarını yorumlarken dikkate alınması gerekmektedir. Kan testinde çıkacak farklılıklar, doğru ve tutarlı kan verme zamanlamasıyla en aza indirilebilmektedir (daha fazla bilgi için bkz. HRT’nin takibi ve izlenmesi) .
Gonadlar cerrahi olarak alınırsa, transfeminenlerde testosteron baskılanması gerekli değildir, bu nedenle; eğer estradiol dozları yüksek veya fizyolojik üstü düzeylerdeyse, dozlar cis kadınlardaki normal fizyolojik seviyelere daha yakın hale gelecek şekilde azaltılması önerilmektedir.
Pogestojenler
Progestojenler, progesteron ve progestinleri içermektedir, progestinler; progesteron veya testosteronun yapısal modifikasyonuyla elde edilen sentetik progestojenlerdir. Farklı yapısal sınıflara ayrılan, çok sayıda ve çeşitli özelliklere sahip onlarca farklı progestin bulunmaktadır (Tablo). Farklı sınıflardaki bazı temel progestinlere örnek olarak; 17α-hidroksiprogesteron türevi olan medroksiprogesteron asetat (MPA; piyasada Tarlusal, Depo-Provera, Divina [mavi tabletlerinde] isimleriyle bulunur), 19-nortestosteron türevi olan noretisteron (NET; piyasada Jineteron, Primolut-N, Activelle, Kliogest, Mesigyna, Trisequens [beyaz tabletlerinde] isimleriyle bulunur), retroprogesteron türevi didrogesteron (piyasada Duphaston olarak bulunur) ve 17α-spirolakton türevi drospirenon (piyasada Angeliq, Yasmin, Drosetil, Drospera, Jerassi, Yazz, Yesdro isimleriyle bulunur) gösterilebilir. Progestinler, progesterona göre ilaç olarak kullanımda daha uygun farmakokinetik özellikler için geliştirilmiştir. Klinik uygulamada kullanılan birkaç progestin, transfeminen HRT’sinde yer almıştır; ancak birkaç istisna dışında progestojenler temel olarak benzer progestojenik etkiler gösterdiğinden dolayı, hemen hemen herhangi bir progestojen de bu amaçla kullanılabilmektedir.
Progestojenler, progestojenik aktiviteleri aracılığıyla antigonadotropik etkilere sahiptir ve hipofizden gonadotropin (LH, FSH) salınımını doz ile bağlantılı olarak baskılarlar. Bunun sonucunda gonadotropin kaynaklı gonadal uyarım azalmaktadır; bu da cinsiyet hormonu üretiminin ve doğurganlığın azalmasıyla sonuçlanmaktadır. Çeşitli progestojenlerin cis erkekler ve transfeminenler üzerindeki doz ile bağlantılı olarak testosteron baskılayıcı etkililiği klinik çalışamlarda tanımlanmıştır (Nieschlag, Zitzmann, & Kamischke, 2003; Nieschlag, 2010; Nieschlag & Behre, 2012; Zitzmann et al., 2017; Aly, 2019). Bunun dikkat çeken örnekleri arasında siproteron asetat (CPA; Wiki), MPA (Wiki), NET (Wiki) ve esteri olan noretisteron asetat (NETA), levonorgestrel (LNG; Zitzmann et al., 2017; Wiki), desogestrel (DSG; Wu et al., 1999; Wiki), dienogest (DNG; Meriggiola et al., 2002; Wiki) ve progesteron (Wiki) gibi bileşikler yer almaktadır. Tek başlarına yüksek doz progestojenler, testosteron düzeylerini ortalama %50—70 oranında baskılayabilmektedirler (Aly, 2019; Zitzmann et al., 2017; Grafik). Bununla birlikte estrojenle kombine edildiklerinde bu baskılama oranı %95’e çıkar ve testosteron seviyeleri cis kadınların sahip oldukları normal aralıklarına iner (Aly, 2019). Progestojenlerin genellikle, cis kadınlardaki yumurta atılmasını durdurmak için gerekli olan dozlarının yaklaşık 5—10 katı düzeyindeki dozlarda maksimum testosteron baskılayıcı kapasitesine ulaştığı görülmektedir (Aly, 2019). Progestojenler arasında, düşük etki gücü ve atipik özellikleri nedeniyle oral progesteron ve didrogesteron bir istisna oluşturur; bu ilaçlar belirgin antigonadotropik etkiye sahip değildir ve testosteron seviyelerini baskılamaları beklenmemektedir (Aly, 2018; Wiki; Wiki).
Transfeminenlerde testosteron baskılanmasına yardımcı olmalarının yanı sıra, progestojenlerin feminenleşme ya da meme gelişimi üzerinde net veya bilinen bir faydası bulunmamaktadır. Bazı transfeminenler, progestojen kullanımıyla meme gelişimlerinin iyileştiğini anekdotal olarak belirtseler de progestojenlerin meme boyutunu veya şeklini iyileştirmedeki rolü literatürde halen tartışmalı bir biçimdedir ve günümüzde teori ya da kanıtlarla desteklenmemektedir (Wiki; Aly, 2020). Özellikle yüksek dozlarda erken dönemde progestojen kullanımının, meme gelişimi üzerinde ters bir etkiye sahip olabileceği olasılığı da mevcuttur (Aly, 2020). Ayrıca birçok transfeminen, progestojenlerin cinsel istek/libido üzerinde olumlu etkileri olduğunu anekdotal olarak belirtmiştir. Ancak mevcut literatürün gözden geçirilmesiyle, progesteron veya progestinlerin insanlarda cinsel isteği/libidoyu olumlu yönde etkilediğine dair bir bulguya rastlanmamıştır (Aly, 2020). Mevcut veriler, progestojenlerin cinsel istek üzerinde nötr bir etkiye sahip olabileceğini veya bunu baskılayabileceğini (özellikle de yüksek dozlarda) düşündürmektedir (Aly, 2020). Bazı kişiler, progesteronun transfeminenlerde duygu durumunu iyileştirebileceğini de öne sürmüştür; ancak bu fikri destekleyen klinik kanıtlar da günümüzde mevcut değildir (Coleman et al., 2022; Nolan et al., 2022). Dikkate değer şekilde, luteal faz seviyelerindeki progesteron, allopregnanolon gibi nörostreoid metaboliteleri nedeniyle cis kadınların yaklaşık %30’unda duygudurumu kötüleştirdiği görünmektedir ve kadınların %2—10’unda ise premenstrüel sendrom (PMS) ve premenstrüel disforik bozukluk (PMDD) tanıları ile kendini gösteren daha belirgin olumsuz etkilere yol açmaktadır (Bäckström et al., 2011; Edler Schiller, Schmidt, & Rubinow, 2014; Sundström-Poromaa et al., 2020). Transfeminenlerde progestojenlerin muhtemel olumlu etkilerini değerlendirmek için daha fazla araştırmaya ihtiyaç vardır.
Klinik kullanımda olan progestojenlerin çoğunda, progestojenik aktivitelerine ek olarak hedef dışı (off-target) ek aktiviteler de bulunmaktadır ve bu aktiviteler arasında istenmeyen sonuçlar elde edilebilmektedir (Kuhl, 2005; Stanczyk et al., 2013; Wiki; Tablo). Progesteronun, nörostreoid niteliği başta olmak üzere, progestinlerle paylaşılmayan çeşitli ek etkileri vardır ve bunlar merkezî sinir sistemi gibi çoklu sistemlerde kendini gösterebilmektedir. MPA ile NET ve türevleri, transfeminenler için istenmeyen bir özellik olan zayıf androjenik aktivite göstermektedirler. NET ve bazı ilişkili progestinler, yüksek dozlarda etinilestradiol (EE) metabolitine dönüşebilir ve bu nedenle EE benzeri estrojenik etkilere (örn. kan pıhtısı ve ilgili kardiyovasküler sorunlarda artış) neden olabilmektedir. Progestojenlerin diğer hedef dışı aktiviteleri arasında antiandrojenik, glukokortikoid ve antimeralokortikoid etkiler bulunmaktadır. Bu ek etkiler, hem HRT etkinliğinde (örn. androjen baskılanması) hem de olası yan etkiler ve sağlık risklerinde farklılıklara yol açabilmektedir. İstenmeyen hedef dışı aktiviteler (androjenik ve glukokortikoid aktivite) içermeyen bazı dikkat çekici progestinler arasında düşük doz CPA, drospirenon (DRSP), dienogest, nomegestrol asetat (NOMAC), didrogesteron ve hidroksiprogesteron kaproat (OHPC) bulunmaktadır. Bununla birlikte, bu progestinler arasında transfeminenlerde kayda değer ölçüde kullanılmakta ve araştırılmakta olan progestin yalnızca CPA’dır.
HRT’de estrojene ek progestojen eklenmesiyle, çeşitli olumsuz sağlık problemlerinin ortaya çıkabileceği bildirilmiştir. Bunlara kan pıhtısı riskinde artış (Wiki; Aly, 2020), koroner kalp hastalığı (Wiki) ve meme kanseri riski (Wiki; Aly, 2020) dahildir. Yüksek doz progestojen kullanımı, ayrıca menenjiomlar ve prolaktinomlar gibi bazı kanser olmayan beyin tümörlerinin riskini de arttırmasıyla ilişkilendirilmiştir (Wiki; Aly, 2020). Koroner kalp hastalığı riskinin, belirli progestojenlerin zayıf androjenik aktivitesinin kan lipid profili üzerindeki etkilerinden kaynaklandığı düşünülebilir; ancak bahsi geçen riskler muhtemelen progestojenik aktiviteye bağlıdır (Stanczyk et al., 2013; Jiang & Tian, 2017). Sağlık risklerinin yanı sıra progestojenler, olumsuz duygudurum değişiklikleriyle de ilişkilendirilmiştir (Wiki; Wiki). Ancak, progesteron ve nörostreoid metabolitleri haricinde bu etkiler tartışmalıdır ve kanıtlarla güçlü biçimde desteklenmemektedir (Wiki; Wiki). Progestojenler genellikle iyi tolere edilir ve çok fazla yan etkiye yol açmadıkları düşünülmektedir.
Bazı progestinlerin aksine, progesteronun istenmeyen hedef dışı aktiviteleri bulunmamaktadır. Androjenik aktiviteye sahip olmadığı için, progesteron kan lipidleri üzerinde olumsuz bir etkiye neden olmaz ve koroner kalp hastalığı riskini arttırması beklenmemektedir. Dikkat çekici biçimde, oral progesteronun estrojene ek olarak eklenmesinin, kan pıhtısı riskini arttırmadığı belirtilmektedir (Wiki). Ayrıca kısa süreli kullanımda, oral progesteronun progestinlere kıyasla daha düşük meme kanseri riskine sahip olduğu düşünülmektedir; ancak bu durumun uzun süreli kullanım için geçerli olmadığı belirtilmektedir (Wiki; Aly, 2020). Dolayısıyla, progesteronun henüz tam olarak açıklığa kavuşturulmamış bazı nedenlerle progestinlere göre daha güvenli bir progestojen olabileceği ve cis kadınlar ile transfeminenlerde HRT için tercih edilebileceği öne sürülmüştür. Ancak bu görüşlere karşı teorik itirazla da mevcuttur. Oral progesteronun tipik dozlarda çok düşük progesteron seviyeleri oluşturduğu ve yalnızca zayıf progestojenik etkilere sahip olduğu bilinmektedir (Aly, 2018; Wiki). Oral progesteronun daha iyi güvenlik profiline sahip olduğu gibi görünen bu durum, gerçekte oluşan progesteron seviyelerinin bir sonucu olabilir ve bu da progestojenik dozla ilişkilidir. Fizyolojik ve tam progestojenik güce sahip dozlarda uygulanan oral olmayan progesteron, sağlık sonuçları bakımından hiçbir zaman uygun şekilde değerlendirilmemiştir ve progestinlerle benzer risklere sahip olması pek olasıdır (Aly, 2018; Wiki).
Feminenleşme ve meme gelişimi üzerindeki etkilerinin belirsizliği ile bilinen ve olası olumsuz etkileri ile riskleri nedeniyle, progestojenler günümüzde transfeminenlerin HRT rejiminde rutin olarak kullanılmamaktadır. Önde gelen trans sağlığı kılavuzları, transfeminenlerde progestojen kullanımıyla ilgili mevcut kanıtların sınırlılıklarına dikkat çekmekte ve kullanımları konusunda çeşitli tutumlar sergilemektedir. Kimi kaynaklar açıkça kullanılmaması önermekte (Coleman et al., 2022—WPATH SOC8), kimileri daha nötr bir yaklaşım benimsemekte (Hembree et al., 2017—Endocrine Society guidelines) ya da kullanımına izin vermektedir (Deutsch, 2016—UCSF guidelines). Bununla birlikte, yukarıdakilere büyük bir istisna, transfeminenlerin HRT’sinde testosteron üretimini baskılamak amacıyla yaygın biçimde kullanılan ve tipik dozlarında güçlü bir progestojen etkisine sahip olan siproteron asetat (CPA) biçiminde karşımıza çıkmaktadır (bkz. Antiandrojenler).
Progestojenlerin çeşitli sağlık riskleri olsa da cis kadınlarda doğal olarak progesteron bulunduğu göz önüne alındığında, sağlıklı genç kişilerde progestojenlerin mutlak risklerinin oldukça düşük olduğu görülmektedir. Örneğin meme kanseri riski gibi bazı riskler, kullanım süresine bağlıdır ve gelişmesi uzun yıllar alabilmektedir. Transfeminenlerde progestojenlerin sağladığı testosteron baskılaması, CPA kullanımından da bilindiği üzere, oldukça yararlı olabilmektedir. Bu bakımdan, örneğin cerrahi olarak gonadların alınmasından önce birkaç yıl testosteron baskılamasına yardımcı olmak amacıyla progestojen almak gibi sınırlı süreli bir kullanımın makul kabul edilebileceği ileri sürülebilmektedir.
Progesteron; transfeminenlerde ağız yoluyla, dil altından, rektal yoldan veya kas içi (IM) veya deri altı yağ dokusuna (SubQ) enjeksiyonlar verilebilir (Wiki). Progestinler ise genellikle oral yol ile kullanılır ancak bazı progestinlerin enjekte edilebilir formları da bulunmaktadır (Wiki).
Oral Progesteron
Progesteron en yaygın olarak oral yol ile alınmaktadır, Türkiye’de piyasada olan Progestan ve Progynex gibi isimler ile satılmakta olup 100 veya 200 mg mikronize progesteron bulunan yağ dolu kapsüller şeklinde sunulmaktadır (Wiki). Yaygın kullanımına rağmen, ileri teknoloji analiz yöntemleriyle (LC—MS) yapılan ölçümlerde oral uygulama yoluyla progesteron seviyelerinin çok düşük (<2 ng/mL [<6,4 nmol/L] – günde 100 mg doz ile) olduğu ve farklı alanlarda tatmin edici progestojenik etki sağlamak açısından yetersiz kaldığı bulunmuştur (Aly, 2018; Wiki). Bu durumla bağlantılı olarak cis erkeklerde yüksek doz oral progesteronun (günde 400mg’a kadar) bile antigonadotropik etki veya testosteron baskılaması göstermediği rapor edilmiştir (Aly, 2018; Wiki). Bu bulgular, enjeksiyon gibi oral olmayan progesteron formları veya progestinler ile karşılaştırıldığında büyük bir zıtlık oluşmaktadır; çünkü bu yöntemler sabit dozlar ve yeterli testosteron baskılanması yapabilmektedirler (Aly, 2019; Wiki).
Oral progesteronun düşük progestojenik gücüne ek olarak, vücutta allopregnanolon ve pregnanolon gibi nörostreoid metabolitlerine aşırı ölçüde dönüştürülmesi söz konusudur. Bu metabolitler güçlü GABAA reseptörü pozitif alosterik modülatörleridir ve uyku hali, bilişsel, bellek ve motor bozukluklar ile duygudurum değişiklikleri gibi fazla alkol kullanımının sonucuna bezner istenmeyen yan etkilere yol açabilmektedir (Wiki; Wiki). Bu yan etkilerden kaçınmak için kullanacak kişilerin oral progesteronu geceleri yatmadan önce almaları tavsiye edilmektedir. Tüm bu nedenlerle pek de pratik olamamasına rağmen, progesteron için oral olmayan yollara başvurulması daha çok tercih edilebilir görünmektedir. Ayrıca oral progesteron kapsülleri rektal uygulama ile alınabilmektedir (bkz. Rektal Progesteron).
Dil Altı (Sublingual) Progesteron
Dil altı progesteron tabletleri Luteina markası adı altında ancak Polonya ve Ukrayna’da bulunmaktadırlar. Teorik olarak oral progesteronun, oral estradiolde olduğu gibi dil altından alınması mümkün olsa da bu ürünler yağ dolu kapsüller halinde formüle edildiği için dil altında kullanımı zor ve rahatsız edici olabilmektedir. Dil altı progesteronla benzer özelliklere sahip olması beklenen bukkal progesteron, geçmişte kullanılmış ancak günümüzde piyasada bulunmamaktadır (Wiki).
Rektal Progesteron
Progesteron, Cyclogest (Türkiye’de piyasadan çekilmiştir) markası adı altında supozituvar şeklinde rektal uygulama için onay almıştır (Wiki) fakat bu ilaç ancak Birleşik Krallık dahil olmak üzere sınırlı sayıda ülkede satılmaktadır (Wiki). Rektal kullanım onayı olmamasına rağmen, oral progesteron kapsülleri oral yol yerine rektal yoldan kullanılabilir ve bu uygulamayala ilk geçiş metabolizmasının çoğundan kaçınıldığından, oral uygulamaya kıyasla çok daha yüksek progesteron seviyeleri elde edilebilmektedir. Oral progesteron kapsüllerinin rektal kullanımı hakkında herhangi bir resmi çalışma bulunmamakla birlikte, bu kapsüller cis kadınlarda vajinal yoldan başarıyla uygulanmış (Miles et al., 1994; Wang et al., 2019) ve vajinal ile rektal yollarının genel olarak benzer farmakokinetik özelliklere sahip olduğu bildirilmiştir (Goletiani, Keith, & Gorsky, 2007; Wiki). Dolayısıyla oral progesteron kapsüllerinin rektal uygulamayla progesteronun etkili bir biçimde alınması için iyi bir teorik temel bulunmaktadır. Oral progesteron çok düşük seviyelerde progesteron sağlerken, rektal progesteron normal luteal faz progesteron seviyelerine kolayca ulaşabilmektedir (Wiki). Ancak sadece yağ dolu kapsül şeklindeki oral progesteron preparatları rektal uygulama ile alınabilmektedirler (örn. Türkiye’de piyasada olan Progestan). Her ne kadar uygulama yolu bazı insanlar için can sıkıcı olsa da, rektal uygulama transfeminenler için progesteronun genel olarak en iyi uygulamaya yolu olarak karşımıza çıkmaktadır.
Enjeksiyon Formundaki Progesteron
Progesteronun enjekte edilebilir formları Türkiye’de piyasa isimleri Progestan Dex, Progynex, Promester ve Prolutex olarak karşımıza çıkmaktadırlar (yurtdışında piyasada Proluton, Progestaject ve Gestone olarak bulunmaktadırlar; Wiki; Prolutex aynı piyasa ismiyle AB ülkelerinde bulunmaktadır; Wiki). Progestan Dex, Progynex, Promester kas içine (IM) enjekte edilmektedirler, öte yandan Prolutex su bazlı bir solüsyon olması sebebiyle deri altı yağ dokusuna (SubQ) enjekte edilebilmektedir (Wiki). Enjeksiyon yolu (IM ya da SubQ) fark etmeksizin, enjekte edilebilir progesteronun süresi nispeten kısadır ve her 1—3 günde bir enjeksiyon yapılmasını gerektirmektedir (Wiki; Wiki). Bu da çoğu kişi için kullanımını fazla zahmetli hale getirmektedir. Estradiolden farklı olarak, progesteron esterlerini (progesteronunun kendisinden daha uzun süre etkili ester biçimlerini) üretmek kimyasal olarak mümkün değildir, çünkü progesteronda esterleştirilmeye imkan tanıyan hidroksil grupları bulunmamaktadır (Wiki). Geçmişte mikro-kristal progesteronun sulu süspansiyon biçimleri piyasada bulunmaktaydı ve 1—2 haftalık etki süresine sahipti; ancak enjeksiyon bölgesinde ağrı gibi sorunlara yol açtıkları dolayısıyla zaman içinde piyasadan kaldırılmışlardır (Aly, 2019; Wiki).
Diğer Progesteron Uygulama Yolları
Transdermal progesteron ve deri altı progesteron implantları gibi başka progesteron uygulama yolları da bilinmektedir; ancak ilaç olarak onaylanmış formları mevcut değildir ve tıpta çok az kullanılmaktadır (Wiki). Bunun nedeni, progesteronun düşük etki gücü ve bu yollarla yeterli düzeyde progesteron seviyesine ulaşmanın zor olmasıdır (Wiki; Wiki). Ayrıca progesteron implantları vücuttan yüksek oranda dışarı atılma (ekstrüzyon) eğilimi göstermektedir (Wiki). Yine de bazı yurtdışında bulunan eczaneler (compounding pharmacies) bu yollarla kullanılabilecek progesteron formları hazırlayabilmektedirler.
Oral ve Enjekte Edilebilir Progestinler
Çoğu progestin, ağız yoluyla alınan katı tabletler şeklinde kullanılır (Wiki), progesterondan farklı olarak; sentetik yapıları sayesinde progestinler bağırsaklarda ve karaciğerde metabolizmaya daha dirençlidir ve yüksek oral biyoyararlanım oranlarına sahiptirler. Ayrıca estrojen reseptörleri durumunun aksine, karaciğerde progesteron reseptörleri minimal düzeydedir ya da hiç bulunmamaktadırlar ve progestojenik aktivitenin karaciğer sentezi üzerindeki ilk geçiş etkisine dair bilinen bir etki yoktur (Lax, 1987; Stanczyk, Mathews, & Cortessis, 2017). Dolayısıyla sadece progestojenik etkisi olan progestinlerde, oral uygulamada belirgin bir sorun görünmemektedir. Ancak bazı progestinler, androjenik, estrojenik ve/veya glukokortikoid aktivite gibi karaciğeri etkileyen hedef dışı (off-target) hormonal özelliklere sahiptir ve bu durum istenmeyen lipid değişiklikleri veya pıhtılaşmayı arttırma (prokoagülasyon) gibi olumsuz etkilere yol açabilmektedir; oral uygulama sürecindeki ilk geçiş etkisiyle bu durum daha da artabilmektedir.
Birçok progestin, kas içi (IM) veya deri altı enjeksiyon (SubQ) için enjekte edilebilir biçimlerde de mevcuttur (Wiki). Yaygın ve bilinen örnekler arasında medroksiprogesteron asetat (MPA), noretisteron enantat (NETE), hidroksiprogesteron kaproat (OHPC) ve algeston asetofenid (dihidroksiprogesteron asetofenid; DHPA) bulunmaktadır (Wiki). Enjekte edilebilir progestinler tek başına kullanılmanın yanı sıra, kombine enjeksiyon kontraseptifleri şeklinde doğum kontrolünde estradiol esterleriyle birlikte de kullanılmaktadır (Wiki). Bu preparatlar özellikle Latin Amerika’daki transfeminenler tarafından HRT amacıyla sıklıkla tercih edilmektedir. Enjekte edilebilir progesteronun etki süresi günlerle ölçülürken, enjekte edilebilir progestinlerin etki süreleri haftalardan aylara kadar değişebilmektedir ve bu nedenle daha seyrek sayıda enjeksiyon gerektirmektedir (Tablo).
Transfeminenler için Kullanılabilen Progestojenler ve Önerilen Dozları
| İlaç | Uygulama Yolu | Form | Doz |
| Progesteron | Oral | Yağ dolu kapsüller | 100–300 mg, günde 1–2 kez |
| Rektal | Supozituvar; Yağ dolu kapsüller | 100–200 mg, günde 1–2 kez | |
| IM enjeksiyon | Yağ solüsyonu | 25–75 mg/1–3 günde bir | |
| Deri Altı (SubQ) enjeksiyon | Su bazlı solüsyon | 25 mg/gün | |
| Progestinler | Oral; IM veya deri altı (SubQ) enjeksiyon | Tabletler; Yağ solüsyonu; Su bazlı solüsyon | Çeşitli |
Farklı formlar, uygulama yolları ve dozlarda progesteron seviyeleri hakkında bilgi için buradaki tabloya (sadece LC–MS ve IA + CS analizleri ile oral progesteron) ve buradaki grafiklere bakılabilir.
Estradiolde olduğu gibi, progesteron seviyeleri konusunda kişiler arasında büyük değişkenlik bulunmaktadır. Öte yandan progestinlerde kişiler arası değişkenlik daha azdır.
Gonadlar cerrahi olarak alındıktan sonra, progestojen dozları cis kadınların fizyolojik seviyelerine yakın olacak şekilde azaltılabilir ya da tamamen kesilebilir.
Türkiye’de oral progesteron olarak, Progestan 100 mg, Progestan 200 mg, Progynex 100 mg bulunmaktadır. Yağ içinde; IM enjeksiyon olarak ise Progestan 50 mg/mL, Progynex 50 mg/mL, Promester 25 mg/mL ve Promester 50 mg/mL bulunmaktadır. Su bazlı; deri altı enjeksiyon olarak ise Progestan Dex 25 mg/1 mL ve Prolutex 25 mg bulunmaktadır. Türkiye’de bulunan oral formuyla karşımıza çıkan Progestan 100mg, Progestan 200mg ve Progynex 100 mg yukarıdaki bölümlerde anlatıldığı rektal olarak da alınabilmektedir.
Antiandrojenler
Estrojenler ve progestojenlerin yanı sıra, transfeminenlerin HRT’sinde kullanılan ve “antiandrojen” (AA) olarak adlandırılan bir başka hormonal ilaç sınıfı daha vardır. Bu ilaçlar, ya androjen üretimini azaltarak (dolayısıyla androjen düzeylerini düşürerek) ya da doğrudan androjenlerin etkilerini engelleyerek vücuttaki androjen etkilerini azaltmaktadır. Farklı etki mekanizmalarıyla çalışmaktadırlar ve bu kapsamda androjen reseptör antagonistleri, antigonadotropinler ve androjen sentez inhibitörleri olarak adlandırılmaktadırlar..
Androjen Reseptör Antagonistleri
Bu ilaçlar, testosteron, DHT ve diğer androjenlerin biyolojik hedef reseptörüne doğrudan bağlanarak etkilerini engellemektedirler. Reseptörlere onları aktive etmeden bağlanırlar, dolayısıyla asıl androjenlerin yerine geçerek bu androjenlerin reseptöre bağlanmasını önlemektedirler. Androjenlerin kompetitif blokörlerinin etki mekanizmaları doğası gereği, bu ilaçların antiandrojenik etkinliği büyük ölçüde doz ile bağlantılıdır ve aynı zamanda kişinin testosteron seviyelerine de temelde bağlıdır. Androjen reseptör antagonistleri arasında spironolakton (Aldactone) gibi streoidal antiandrojenler (SAA), siproteron asetat (CPA; Androcur) ve bikalutamid (Casodex) gibi nonsteroidal antiandrojenler (NSAA) bulunmaktadır.
Antigonadotropinler
Bu ilaçlar, hipofiz bezinde GnRH aracılığıyla salınan gonadotropinleri baskılayarak gonadların androjen üretimini azaltmaktadırlar. Estrojenler ve progestojenler de bu etki mekanizmasına dahildir. Ayrıca löprolid (leuprorelin; Lucrin) ve elagoliks (Orilissa) gibi GnRH agonistleri de benzer mekanizmayla çalışarak antigonadotropik etki göstermektedir.
Androjen Sentez İnhibitörleri
Enzim aracılığıyla gerçekleşen androjen sentezini engellemektedirler. Finasterid (Proscar) ve dutastreid (Avodart) gibi 5α-redüktaz inhibitörleri (5α-RI’lar) buna örnektir. Bunun yanı sıra ketokonazol (Ketoral) ve abirateron asetat (Abiratex) gibi güçlü 17α-hidroksilaz/17,20-liaz inhibitörleri de mevcuttur; ancak toksisite, yüksek maliyet ve deneyim eksikliği gibi nedenlerle transfeminenlerin HRT’sinde kullanılmazlar.
Antigonadotropinler ve androjen sentez inhibitörleri, androjen seviyelerini düşürmeleri sayesinde ikincil bir etki olarak antiandrojenik etki gösterirler bu sebeple genellikle (özellikle literatürde) “antiandrojen” olarak adlandırılmazlar. Bu terim çoğunlukla, spesifik olarak androjen reseptör antagonistlerini tanımlamak için kullanılır. Bununla birlikte, antigonadotropinler ve androjen sentez inhibitörleri de bir bakıma antiandrojen etkisi sergilediklerinden ve daha fazla karışıklığı önlemek adına “antiandrojen” şeklinde tanımlanmıştır.
Cerrahi operasyon ile gonadlar alındıktan sonra (orşiektomi ya da vajinoplasti sonrası) antiandrojenler kullanılmamalıdır. Eğer gonad kaynaklı testosteron baskılandığı halde akne, sebore veya androgenetik alopesi (erkek tipi kellik) gibi istenmeyen androjen bağımlı semptomlar devam ediyorsa, daha düşük dozda bir androjen reseptör antagonisti (örn. günlük 100—200 mg spironolakton veya 12,5—25 mg bikalutamid) bu semptomları tedavi etmek amacıyla sürdürülmeye devam edilebilir.
Transfeminenler için Kullanılabilen Antiandrojenlerin (Androjen Reseptör Antagonistlerin) Mevcut Formları ve Önerilen Dozları
| İlaç | Tür | Uygulama Yolu | Form | Doz |
| Siproteron asetat(CPA) | Progestojen; Androjen reseptör antagonisti | Oral | Tablet | 2,5–12,5 mg/güna |
| Spironolakton | Androjen reseptör antagonisti; Zayıf androjen sentez inhibitörü | Oral | Tablet | 100–400 mg/günb,c |
| Bikalutamid | Androjen reseptör antagonisti | Oral | Tablet | 12,5–50 mg/günb |
aCPA için bu doz aralığı, 50mg’lik bir tabletin dörtte birinin gün aşırı ya da 2—3 günde bir alınması (4,2—12,5 mg/gün) şeklindedir. 6,25—12,5 mg/gün dozları, maksimum testosteron baskılanmasını sağlamak için yeterlidir; daha düşük dozlar daha az etkili olabilmektedir (Aly, 2019).
bSpironolakton ve bikalutamid için, testosteron seviyelerinin önemli ölçüde baskılandığı (≤200 ng/dL [<6,9 nmol/L]) varsayılmaktadır. Bu aralığa kadar baskılanmamış testosteron seviyelerinde daha yüksek dozlar gerekli olabilmektedir.
cSpironolaktonun ve matabolitlerinin yarılanma ömrü tablodaki diğer ilaçlara göre daha kısadır; bu sebeple günlük dozu 2’ye bölerek (örn. sabah ve akşam [12 saatte bir] 100—200 mg) almak önerilmektedir.
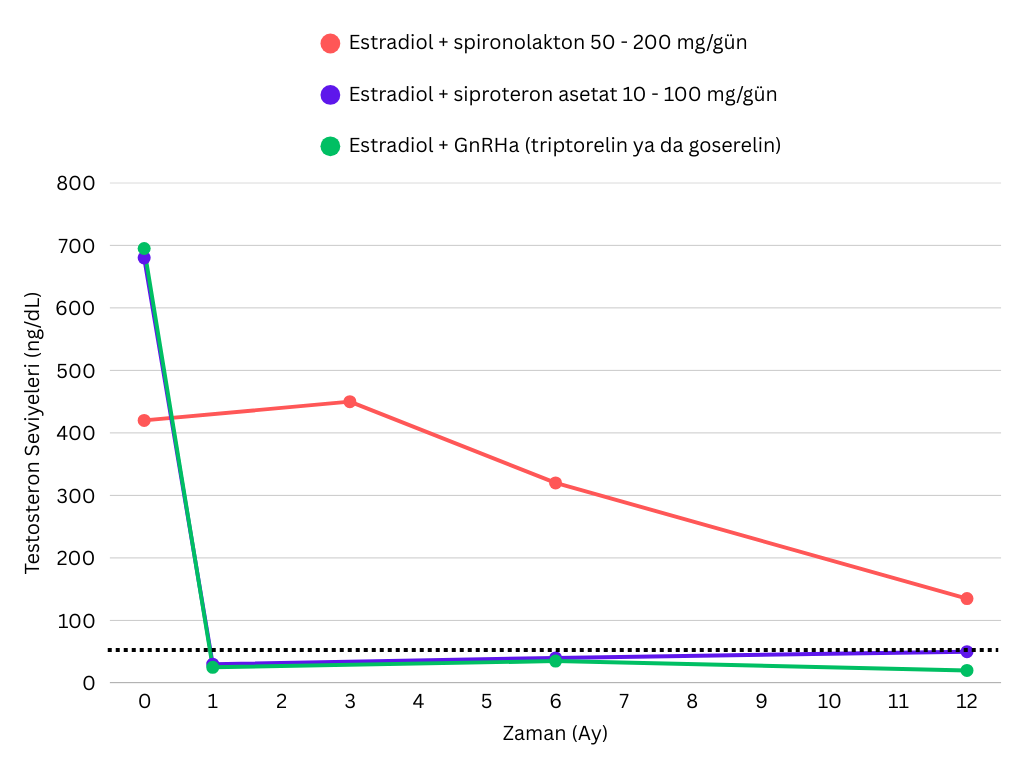
Transfeminenlerde bir yıllık HRT boyunca estradiol ile birlikte farklı antiandrojenlerin kullanılması sonucu gonadal testosteron üretimi ve dolaşımdaki testosteron düzeylerinin (ng/dL) baskılanmasını gösteren tablo yukarıda verilmiştir (Sofer et al., 2020). Estradiol formları, günde 2—8 mg oral tablet, 2.5—5 mg transdermal jel ve 50—200 μg transdermal bant şeklinde olarak belirtilmiştir. Anti androjenler arasında günde 50—200 mg spironolakton (n=16), siproteron asetat (n=41) ve GnRH agonistleri (enjeksiyon ile ayda bir 3,75 mg triptorelin veya 3,6 mg goserelin) (n=10) bulunmaktadır (Sofer et al., 2020). Kesik yatay çizgi, cis kadınlarda normal kabul edilen testosteron seviyesinin üst sınırını belirtmektedir.
Siproteron asetatın (CPA) daha düşük dozlarının (10—12,5 mg/gün), daha yüksek dozlarla (25—100 mg/gün) eşdeğer testosteron baskılaması sağladığı ve daha yüksek dozların artık kullanılmaması gerektiği (Aly, 2019) unutulmamalıdır.
Androjen Reseptör Antagonistleri
Siproteron Asetat (CPA)
Siproteron asetat (CPA; Androcur), hem progestojen hem de antiandrojen özelliğe sahip bir ilaçtır. Cis kadınlarda, hormonal doğum kontrolü (hormonal kontraseptif) ve menopoz hormon tedavisi de dahil olmak üzere yaygın biçimde progestojen olarak kullanılmaktadır. Ayrıca, cis kadınlarda akne, hirsutizm (fazla yüz/vücut kılı), androgenetik alopesi (erkek tipi kellik) ve polikistik over sendromuna (PCOS) bağlı hiperandrojenizm gibi androjen-bağımlı durumları tedavi etmek için, cis erkeklerde ise prostat kanseri ve cinsel dürtünün kontrol altına alınması hedefiyle cinsel bozukluklarının (parafililer, hiperseksüalite, suç unsuru taşıyan cinsel aktiviteler vb.) tedavisi için antiandrojen olarak kullanılır. Transfeminenlerde HRT’nin önemli bir bileşeni olarak (antiandrojen) CPA dünyanın pek çok yerinde en yaygın kullanılan antiandrojen ilaçlardan birisidir. Ek olarak CPA, ABD’de bulunmamakta olup, dünyanın o kısmında spironolakton tercih edilmektedir. Avrupa’da ve muhtemelen dünya genelinde transfeminenlerde en sık kullanılmakta olan antiandrojen ise CPA’dır (T’Sjoen et al., 2019; Glintborg et al., 2021; Coleman et al., 2022).
Etki mekanizması ve Dozlar
CPA, güçlü bir progestojen olarak gonadotropin salımını baskılamaktadır ve böylece testosteron düzeylerini düşürmektedir. Ayrıca androjen reseptörlerinde antagonistik etki (bloklama) gösterir (Aly, 2019). Ancak CPA’nın progestojenik gücü, androjen reseptör antagonizmasından çok daha fazladır (Aly, 2019). Cis kadınlarda progestojen olarak kullanılan CPA dozu genellikle 2 mg/gündür ve bu doz, fizyolojik luteal faz progesteron seviyelerine denk gelen etkiler (örn. gonadotropin baskılanması, ovülasyonun engellenmesi, endometriumda değişimler ve korunma) sağlar (Aly, 2019). Buna karşılık, androjen-bağımlı hastalıkların tedavisinde ise geleneksel olarak 50—300 mg/gün gibi çok daha yüksek dozlar kullanılmıştır (Aly, 2019).
Transfeminenlerde tarihsel olarak 50—150 mg/gün aralığında kullanılan CPA dozları son yıllarda büyük ölçüde düşmüş ve 10—12,5mg/günü aşmayan dozlar önerilmektedir (Aly, 2019; Coleman et al., 2022—WPATH SOC8). Bu daha düşük dozlar, daha yüksek dozlar ile eşdeğer biçimde güçlü progestojenik etki göstermektedirler ve estradiol ile birlikte kullanıldığında testosteron seviyelerini aynı derecede baskılamaktadır (Aly, 2019; Meyer et al., 2020; Even Zohar et al., 2021; Kuijpers et al., 2021; Coleman et al., 2022). Günümüzde 5—6,25 mg/gün gibi daha da düşük dozların da halen tam etkili olup olmadığını araştıran çalışmalar sürmektedir (Aly, 2019).
Testosteron Baskılaması
Estrojen olmadan tek başına kullanılan CPA, testislere sahip bireylerde testosteronu ortalama %50—70 oranında baskılayarak düzeyleri yaklaşık 150—300 ng/dL (5,2—10,4 nmol/L) aralığına düşürmektedir (Meriggiola et al., 2002; Toorians et al., 2003; Giltay et al., 2004; T’Sjoen et al., 2005; Tack et al., 2017; Zitzmann et al., 2017; Aly, 2019). Düşük dozlar (örn. 10mg/gün), yüksek dozlar (örn. 50—100mg/gün) ile aynı düzeyde testosteron baskılaması sağlamaktadır ve bu durum, CPA’nın antigonadotropik etkilerinin daha düşük terapötik dozlarda bile maksimuma ulaştığını göstermektedir (Aly, 2019).
Tek başına (estradiol olmadan) CPA, dozdan bağımsız olarak testosteronu cis kadın aralığına (<50 ng/dL [<1,7 nmol/L]) indirememektedir. Buna rağmen CPA’nın düşük doz estradiol ile birlikte kullanımı testosteron seviyelerini düzenli olarak cis kadın aralığına baskılayabilmektedir (Aly, 2019; Angus et al., 2019; Gava et al., 2020; Sofer et al., 2020; Collet et al., 2022). Fakat, bu istenen etki için kişinin ortalama 60 pg/mL (220 pmol/L) gibi belli bir estradiol düzeyine ulaşması gerekebilmektedir (Aly, 2019). Estradiol dozunun çok düşük kalması durumunda—CPA olsa dahi—tam testosteron baskılanması sağlanamayabilmektedir (Aly, 2019).
Androjen Reseptör Antagonizması ve Doz Etkisi
Testosteron baskılama etkisine ek olarak CPA, doz-bağımlı bir şekilde androjen reseptör blokajı yapabilse de bunun anlamlı düzeyde gerçekleşmesi için (örn. 50–300 mg/gün gibi) daha yüksek dozlar gereklidir (Aly, 2019). Düşük dozlarda (≤12,5 mg/gün) anlamlı bir reseptör blokajı sağlanamayabilir ve bu dozlar esasen progestojenik etki ile sınırlı kalabilir (Aly, 2019). Dolayısıyla, güncel “düşük doz” yaklaşımında CPA’yı “antiandrojen” olarak adlandırmak yerine “progestojen” olarak adlandırmak daha yerinde olabilmektedir. Ayrıca12,5 mg/gün dozundan daha yüksek dozlar, büyük ölçüde progestojenik aşırı doz riski nedeniyle artık güvenli kabul edilmez ve transfeminenlerde önerilmemektedir. Ayrıca, CPA (~10 mg/gün) ve estradiol kombinasyonu, testosteron seviyelerini cis kadın aralığına kadar baskıladığından dolayı ek olarak androjen reseptör blokajına klinik anlamda gerek yoktur (Aly, 2019).
Yan Etkiler ve Riskler
CPA ile bildirilen bazı yan etkiler arasında yorgunluk, kilo artışı (Belisle & Love, 1986; Hammerstein, 1990; Martinez-Martin et al., 2022) ve testosteron baskılanmasının sonucu olarak olası ek cinsel işlev bozuklukları (örn. cinsel istekte azalma) bulunmaktadır (Wiki; Aly, 2019). Ayrıca depresyon ve duygudurum değişiklikleri riski nadiren de olsa bulunmaktadır (Wiki). CPA, transfeminenlerde gebelik benzeri meme değişikliklerine (örn. lobuloalveoler gelişim) yol açabildiği bildirilmiştir (Kanhai et al., 2000) ve bazen laktasyon (süt salgısı) ortaya çıkabilmektedir (Gooren, Harmsen-Louman, & van Kessel, 1985; Schlatterer et al., 1998; Bazarra-Castro, 2009).
Projestojenler—özellikle CPA gibi yüksek dozlarda—erken dönemde kullanımının meme gelişimi üzerinde olumsuz etki yaratabileceğine dair endişeler dile getirilmiştir (Aly, 2020). Ancak, şu anda bu endişeleri destekleyecek insanlar ile yapılmış çok az veri bulunmaktadır. CPA’nın yan etkilerinin doza bağlı olduğu düşünülmekte ve en düşük etkili dozların kullanılmasının yan etkileri en aza indireceği varsayılmaktadır.
CPA, diğer progestojenler gibi, meme kanseri (Fournier, Berrino, & Clavel-Chapelon, 2008; CGHFBC, 2019; de Blok et al., 2019; Aly, 2020; Wiki) ve kan pıhtısı (Seaman et al., 2007; Connors & Middeldorp, 2019; Aly, 2020; Wiki) riskini artırmaktadır. Daha yüksek dozlarda CPA, prolaktin seviyelerinde artış (Sofer et al., 2020; Wilson et al., 2020; Wiki) ve prolaktinomlar (McFarlane, Zajac, & Cheung, 2018; Nota et al., 2018; Wiki) ile menenjiomlar (McFarlane, Zajac, & Cheung, 2018; Nota et al., 2018; Millward et al., 2021; Weill et al., 2021; Aly, 2020; Wiki) gibi kanser olmayan beyin tümörlerinde artmış riskle ilişkili bulunmuştur. Bu risklerin doz-bağımlı olduğu düşünülmektedir; dolayısıyla düşük dozlarda riskin asgariye indirildiği varsayılmaktadır.
Yüksek dozlarda CPA, karaciğer üzerinde zayıf da olsa androjenik etkilere yol açarak HDL (“iyi”) kolesterolün azalmasına ve uzun vadede potansiyel koroner kalp hastalığı riskini artırabilen olumsuz lipid profili değişikliklerine neden olabilmektedir (Coleman et al., 2022; Wiki). Ayrıca yüksek doz CPA’nın kan basıncında artış ve insülin direncinde yükseliş gibi muhtemel olumsuz etkileri de rapor edilmiştir (Martinez-Martin et al., 2022). Bunun yanında, 25–50 mg/gün seviyelerinde kullanılan CPA’nın anormal karaciğer fonksiyon testleri (yüksek ALT ve AST) ve nadiren de olsa karaciğer toksisitesi (hepatotoksisite) vakalarıyla ilişkilendirildiği bildirilmiştir (Heinemann et al., 1997; Bessone et al., 2016; Kumar et al., 2021; Wiki; Table). Günlük 20 mg’ın altındaki dozlarda karaciğer fonksiyon bozukluğunun ve de muhtemelen karaciğer toksisitesinin çok daha az görüldüğü gözlemlenmiştir (Wiki). CPA ile klinik olarak anlama sahip 100’den fazla karaciğer toksisitesi vakası bildirilmiştir, ancak 50 mg/gün veya daha düşük dozlarda CPA ile sadece iki vaka bildirilmiştir (Wiki; Table).
CPA kullanan kişilerde prolaktin düzeylerinin (prolaktinoma tespiti için) ve karaciğer fonksiyonlarının izlenmesi önerilmektedir. Ayrıca olası menenjiomların tespiti için düzenli beyin MRG (MRI) taraması önerilmektedir (özellikle ≥10 mg/gün CPA kullananlarda) (Aly, 2020).
Kullanım Yolu
CPA genellikle tablet (10, 50 ve 100 mg) formunda bulunur ve oral yoldan alınır (Wiki). Türkiye’de 50 ve 100mg CPA içeren tabletler Androcur markası adı altında satılmaktadır. Bazı ülkelerde Androcur Depot adıyla 300 mg’lık uzun etkili bir enjeksiyon formu mevcuttur (Türkiye’de mevcut değildir) ancak transfeminenlerde yaygın kullanılmaz ve yüksek doza maruz kalma ile sonuçlanır (Wiki). Düşük doz elde etmek için tabletleri dörde bölmek (örn. 50 mg tabletten 4 adet 12,5 mg doz) mümkündür. Tabletleri daha kolay ve zahmetsizce dörde bölmek için eczanelerde ya da alışveriş sitelerinde satılan hap kesici/kırıcı kullanımı önerilmektedir. CPA’nın ortalama yarı ömrü 1,6 ila 4,3 gün arasındadır (Wiki; Aly, 2019) ve günde bir kez veya iki-üç günde bir alınabilir (Aly, 2019). Dolayısıyla ilaç kesintisiz olarak kandaki seviyelerini koruyabilir ve doz aralıklarını açarak daha düşük dozlar sağlamak da mümkündür.
?) Diğer Progestojenlerin Kullanımına Gerek Var mı?
Daha önce de belirtildiği üzere, CPA transfeminen kişilerde şu anda kullanılan nispeten düşük dozlarda bile (örn. 5—12,5 mg/gün) güçlü bir projestojendir. Bu nedenle, CPA kullanan transfeminenlerin (özellikle progestojenik etkileri oluşturma nedeniyle) ek bir progestojen (örn. progesteron) kullanmasına gerek yoktur. Bu, CPA kullanan kişilerde sıklıkla gözden kaçırılan bir durumdur ve maliyet/yan etki profilinde artışa yol açarken olası bir ek fayda sağlamamaktadır.
Spironolakton
Spironolakton (Aldactone), hem antiandrojen hem de antimineralokortikoid özelliklere sahip bir ilaçtır. Akne, hirşutizm, androgenetik alopesi (erkek tipi kellik) gibi androjen-bağımlı deri/kıl sorunlarını tedavi etmek amacıyla cis kadınlarda, PCOS’a bağlı hiperandrojenizm tedavisinde ve ayrıca transfeminenlerin HRT’sinde bir bileşen olarak yaygın biçimde kullanılır. Özellikle ABD’de transfeminenlerde en sık tercih edilen antiandrojen spironolaktondur. Antimineralokortikoid etkisi sebebiyle orijinal kullanım alanı kalp yetmezliği, hipertansiyon, yüksek mineralokortikoid seviyeleri, hipokalemi (potasyum eksikliği) ve nefrotik sendrom, asit (ascites; karın boşluğunda aşırı miktarda sıvı birikmesi) gibi ödemler olan hastalıklardır (Wiki).
Antiandrojenik etkileri bakımından spironolakton, zayıf bir androjen reseptör antagonisti ve aynı zamanda zayıf bir androjen sentez inhibitörüdür (17α-hidroksilaz ve 17,20-liyaz enzimlerini kısmen inhibe eder) (Wiki). Bununla birlikte, anlamlı düzeyde progestojenik etkisi, 5α-redüktaz inhibisyonu veya direkt estrojenik aktivitesi olduğu düşünülmez (Wiki). Buna rağmen, yeterince yüksek dozlarda antiandrojenik etki sağlayabilmesi dolayısıyla estrojen benzeri etkiler (örn. meme büyümesi) gözlemlenebilmektedir (Wiki).
Testosteron Baskılaması ve Etkinlik
Spironolaktonun testosteron seviyeleri üzerindeki etkileri, cis erkekler, cis kadınlar ve transfeminenlerde yapılan klinik araştırmalarda zayıf ve tutarsız bulunmuştur. Çoğu çalışma spironolaktonun testosteron seviyelerini değiştirmediğini, bazıları ise azalttığını, az sayıda çalışma ise artırdığını bildirmiştir (Aly, 2018). Buna rağmen, testosteron seviyesinde değişim olmaksızın dahi antiandrojenik etki (androjen reseptör blokajı) sağlayabildiği gösterilmiştir. Dolayısıyla spironolaktonun esas antiandrojenik mekanizması androjen reseptör blokajıdır.
Transfeminenlerde spironolakton kullanımında, testosteron baskılamasını esasen estrojen sağlamaktadır. Nitekim spironolakton + estradiol ile estradiol tek başına kıyaslayan çalışmalar (örn. Leinung, 2014; Leinung, Feustel, & Joseph, 2018; Angus et al., 2019) ve spironolaktonun farklı dozlarını kıyaslayan çalışmalar (örn. Liang et al., 2018; SoRelle et al., 2019; Allen et al., 2021) bu sonucu desteklemektedir. Spironolakton; birçok transfeminende testosteronu cis kadın aralığına düşürecek kadar baskılayamaz ve testosteron sıklıkla 50–450 ng/dL (1,7–15,6 nmol/L) gibi daha yüksek seviyelerde gözlemlenebilmektedir (Leinung, 2014; Leinung, Feustel, & Joseph, 2018; Liang et al., 2018; Angus et al., 2019; Jain, Kwan, & Forcier, 2019; SoRelle et al., 2019; Sofer et al., 2020; Burinkul et al., 2021). Buna karşın testosteron seviyelerinde zamanla kademeli bir düşüş de görülebilmektedir (örn. Liang et al., 2018; Sofer et al., 2020 [Grafik]; Allen et al., 2021).
Klinik olarak, spironolaktonun androjen reseptör blokajı gücü nispeten zayıftır ve daha çok düşük veya cis kadın aralığına yakın testosteron seviyelerini bloklamak için uygundur (Aly, 2018). Bu, 50–200 mg/gün spironolakton kullanan sağlıklı cis kadınlar ile PCOS’lu cis kadınlarda kullanan doz ayarlama çalışmalarına (Goodfellow et al., 1984; Lobo et al., 1985; Hammerstein, 1990; James, Jamerson, & Aguh, 2022) ve daha güçlü bir antiandrojen olan flutamid ile karşılaştırma yapılan çalışmalara (Cusan et al., 1994; Erenus et al., 1994; Shaw, 1996) dayanmaktadır. Transfeminenlerde spironolaktonun klinik olarak antiandrojenik etkinliği henüz çok sınırlı incelenmiştir (Angus et al., 2021). Androjen-bağımlı saç ve cilt problemlerine sahip cis kadınlarda spironolaktonun antiandrojenik etkinliği kanıtlanmış ve literatürde sağlam bir zemine sahiptir; dolayısıyla, testosteron seviyelerinin çok yüksek olmadığı durumlarda spironolaktonun işe yaradığı bilinmektedir (Brown et al., 2009; van Zuuren & Fedorowicz, 2016; Layton et al., 2017; Barrionuevo et al., 2018; James, Jamerson, & Aguh, 2022). Yüksek testosteron seviyeleri için daha yüksek doz (örn. 300–400 mg/gün) spironolakton önerilmekte olup trans sağlığı kılavuzlarınca da bu durum kabul görmektedir (Aly, 2020).
→ Özetle, spironolakton nispeten zayıf bir antiandrojendir ve birçok transfeminende testosteronun tam baskılanmasını sağlamayabilir. Bu nedenle, istenen maskülen özelliklerin gerilemesi, feminenleşme ve meme gelişimi beklenen seviyede olmayabilmektedir.
→Bikalutamid, CPA, GnRH modülatörleri ve yüksek doz estradiol monoterapisi gibi alternatif yaklaşımlar, testosteron seviyelerini daha güvenli biçimde ve daha etkin bir şekilde düşürme veya androjen reseptörlerini daha güçlü bloklama kapasitesine sahiptir.
→Eğer kişide estradiol + spironolakton kombinasyonunda testosteron seviyesi halen yüksek bir seyirde ise, farklı bir antiandrojene geçilmesi, estradiol dozunun yükseltilmesi ya da antigonadotropik gücü olan bir progestojen (örn. oral olmayan progesteron veya progestin) eklenmesi tavsiye edilmektedir.
Antimineralokortikoid Etkiler ve Yan Etkiler
Spironolakton, güçlü bir antimineralokortikoiddir, mineralokortikoid steroid hormonları olan aldosteron ve 11-deoksikortikosteronun biyolojik hedefi olan mineralokortikoid reseptörünün bir antagonistidir. Progesteron da antimineralokortikoid etkiye sahiptir ancak spironolakton bu bakımdan çok daha güçlüdür. Mineralokortikoid reseptörleri diğer görevlerinin yanı sıra elektrolit ve sıvı dengesini düzenlemede rol alır; spironolakton, antimineralokortikoid aktivitesinin faydalı bir etkisi olarak kabul edilebilecek kan basıncında hafif bir düşüş ile ilişkilidir (Martinez-Martin et al., 2022).
Genellikle iyi tolere edilse de spironolakton, çok düşük tansiyon seviyeleri, baş dönmesi, yorgunluk, sık idrara çıkma ve yükselmiş kortizol gibi antimineralokortikoid yan etkilere neden olabilmektedir (Kellner & Wiedemann, 2008; Kim & Del Rosso, 2012; Zaenglein et al., 2016; Layton et al., 2017; James, Jamerson, & Aguh, 2022). Bazı çevrelerde spironolaktonun antimineralokortikoid etkisinin ve artmış kortizol seviyelerin, transfeminenlerde visseral yağ dokusu artışına neden olabileceği öne sürülmüştür fakat bu iddiayı destekleyen bir kanıt bulunmamaktadır (Aly, 2020). Mevcut veriler ayrıca, spironolaktonun transfeminenlerde meme gelişimini engellediğine veya ciddi nöropsikiyatrik etkilere yol açtığına dair bir bilgi sunmamaktadır.
Spironolaktonun antimineralokortikoid aktivitesine bağlı olarak ortaya çıkan en önemli risk hiperkalemidir (yüksek potasyum düzeyleri) (Wiki). Bu komplikasyon nadir görülmektedir ve çoğunlukla belirli risk faktörlerine sahip kişilerle sınırlıdır ancak ciddi olabilmektedir ve hastanede yatış ya da ölüme yol açabilmektedir. Hiperkalemi için risk faktörlerine sahip olan kişilerin spironolakton aldıkları esnada kan potasyum düzeylerini düzenli olarak takip ettirmesi önerilmektedir, ancak risk faktörleri bulunmayan kişilerde gerekli görünmemektedir (Plovanich, Weng, & Mostaghimi, 2015; Zaenglein et al., 2016; Layton et al., 2017; Millington, Liu, & Chan, 2019; Wang & Lipner, 2020; Gupta et al., 2022; Hayes et al., 2022). Hiperkalemi için risk faktörleri arasında ileri yaş (>45 yaş), azalmış böbrek fonksiyonları, diğer potasyum yükselten ilaçların eş zamanlı kullanımı ve potasyum takviyeleri veya potasyum içeren tuz muadilleri alınması yer alır. Öneme sahip diğer potasyum yükselten ilaçlar arasında, potasyum tutucu diüretikler (örn. amilorid, triamteren [Trianseril] ve diğer antimineralokortikoidler), ACE inhibitörleri, anjiyotensin II reseptör blokerleri ve trimetoprim (bakteriyel enfeksiyonlar için kullanılan bir antibiyotik; Bactrim, Kemoprim, Metoprim, Trimoks) gibi ilaçlar bulunur (Kim & Rosso, 2012; Salem et al., 2014). İlaç etkileşimine örnek olarak, >65 yaş üzerindeki yaşlı kişiler spironolakton ile trimetoprim birlikte alındıklarında ciddi hiperkalemi ve ani ölüm meydana gelebilmektedir (Antoniou et al., 2011; Antoniou et al., 2015).
Hiperkalemi riski taşıyan kişilerde, potasyum açısından zengin gıdaların alımını sınırlamak amacıyla genellikle diyet kısıtlaması önerilmektedir (Roscioni et al., 2012; Cupisti et al., 2018). Trans sağlığında bu durum sıklıkla, potasyumun yüksek olduğu söylenen muz gibi yiyeceklerin tüketilmemesi yönünde tavsiyeler olarak karşımıza çıkmaktadır. Ancak spironolakton ile hiperkalemiden kaçınmak için diyetle potasyum alımını sınırlamak tamamen teoriktir ve aslında kanıta dayalı değildir; şu ana dek elde edilen veriler bu uygulama/tavsiyenin etkinliğini desteklememektedir (St-Jules, Goldfarb, & Sevick, 2016; St-Jules & Fouque, 2021; Babich, Kalantar-Zadeh, & Joshi, 2022; St-Jules & Fouque, 2022). Dolayısıyla, spironolakton kullanımı sırasında rutin diyetle potasyum kısıtlaması gerekli değildir.
Spironolaktonun antimineralokortikoid aktivitesinin yanı sıra, PCOS’lu (polikistik over sendromu) cis kadınlarda LDL (“kötü”) kolesterol düzeylerini arttırdığı ve HDL (“iyi”) kolesterol düzeylerini düşürdüğü bildirilmiştir (Nakhjavani et al., 2009). Bununla birlikte, bazı çalışmalar spironolakton ile kolesterol düzeylerinde olumsuz bir etki bulmadığından sonuçlar çelişkili görünmektedir (Polyzos et al., 2011). Uzun vadede, kolesterol düzeyleri üzerindeki olumsuz etkiler koroner kalp hastalığı riskinde artışa yol açabilmektedir.
Spironolakton oral yoldan tablet formunda (örn. 25, 50 ve 100 mg) alınır (Wiki). 7α-tiyometilspironolakton, 6β-hidroksi-7α-tiyometilspironolakton ve kanrenon (7α-desthioasetil-δ6-spironolakton) gibi çeşitli aktif metabolitlerin bir ön ilacıdır (Wiki). Spironolakton ve bu aktif metabolitlerin eliminasyon yarı ömürleri sırasıyla 1,4 saat, 13,8 saat, 15 saat ve 16,5 saattir (Wiki). Spironolakton ve aktif metabolitleri ile ilaç düzeylerinin nispeten kısa süresi olması (Grafik) nedeniyle, günlük spironolaktonun dozunun günde ikiye bölünerek alınması, günde tek doz almaktan daha optimaldir ve bu yönde tavsiyeler verilmektedir (Reiter et al., 2010).
Bikalutamid
Bikalutamid (Casodex), güçlü ve oldukça seçici bir androjen reseptör antagonisti olarak etki gösteren steroid yapıda olmayan bir antiandrojendir (NSAA) (Wiki). Temel olarak cis erkeklerdeki prostat kanserinin tedavisinde kullanılmaktadır. Prostat kanseri androjen bağımlı bir kanser türüdür ve antiandrojenler, bu kanserin ilerlemesini yavaşlatmaya yardımcı olabilmektedir. Bu durum bikalutamid’in reçetelenme sebeplerinin büyük çoğunluğunu oluşturmaktadır (Wiki). Prostat kanserine ek olarak, daha az sıklıkta da olsa, bikalutamid; cis kadınlarda hirsutizm (aşırı yüz/vücut kullanması), androgenetik alopesi (erkek tipi kellik) ve PCOS (polikistik over sendromu) tedavisinde, periferik veya gonadotropin bağımsız erken puberte (GnRH agonistlerinin etkili olmadığı nadir bir puberte prekoks türü) yaşayan cis erkek çocuklarda ve priapizm yaşayan cis erkeklerde kullanılmaktadır (Wiki).
Bikalutamid ayrıca transfeminen kişilerde antiandrojen olarak giderek daha fazla benimsenmektedir (Aly, 2020; Wiki). Bununla birlikte, trans sağlığı alanındaki saygın ve önde gelen rehberler, ya bikalutamid kullanımını önermemekte (Deutsch, 2016—UCSF guidelines; Coleman et al., 2022—WPATH SOC8) ya da kullanımına ancak temkinli şekilde izin vermektedir (Thompson et al., 2021—Fenway Health guidelines). Bunun sebebi, transfeminen kişilerde bikalutamid üzerine yapılan çalışmaların yetersizliği ve potansiyel riskleridir. (Neyman, Fuqua, & Eugster, 2019).
Bikalutamid, spironolakton veya CPA’dan çok daha güçlü bir androjen reseptör antagonisti olarak karşımıza çıkmaktadır (Wiki; Neyman, Fuqua, & Eugster, 2019). Transfeminen kişilerde tipik olarak 25—50mg/gün dozlarında kullanılır; ancak bu dozlar yeterli klinik veri bulunmadığından dolayı herhangi bir dayanağa sahip değildir. Yine de androjen reseptör blokajındaki göreceli yüksek gücü ve estradiolün eşzamanlı olarak testosteron düzeylerini baskılaması sayesinde, bu dozlar birçok transfeminen kişi için testosteron blokajında oldukça yeterli olabilmektedir. Daha yüksek dozlarda (>50 mg/gün), bikalutamidin tek başına cis erkek aralığındaki testosteron seviyelerini (>300 ng/dL [>10,4 nmol/L]) önemli ölçüde bloke edebildiği, prostat kanseri olan cis erkeklerde bikalutamid monoterapisini ele alan çalışmalardan bilinmektedir (Wiki). Bunu spironolakton ve CPA aynı şekilde yapamamaktadır. Androjen reseptörüne seçiciliği nedeniyle bikalutamidin hormonal açıdan başka bir hedefe yönelik aktivitesi (off-target activity) yoktur ve cis kadınlarda neredeyse hiç yan etki oluşturmamaktadır (Wiki; Erem, 2013; Moretti et al., 2018). Bikalutamidin, cis kadınlarda hirsutizm için kullanıldığı titiz bir klinik çalışmada gözlemlenen tek belirgin yan etki, total ve LDL (“kötü”) kolesterol düzeylerinde bir artış olduğu yönündedir (Moretti et al., 2018). Bu nedenle bikalutamid genellikle oldukça iyi tolere edilmektedir. Hedef dışı hormonal etkileri olmayan saf bir androjen reseptör antagonisti olan bikalutamid, bu yönüyle spironolakton ve CPA gibi ek hormonal etkiler (örn. antimineralokortikoid veya güçlü progestojenik etki) ve buna bağlı yan etkiler ile barındırdığı risklerden farklılık göstermektedir.
Seçici bir androjen reseptör antagonisti olarak bikalutamid, tek başına kullanıldığında testosteron üretimini veya seviyelerini düşürmek yerine arttırmaktadır (Wiki). Bunun nedeni, gonadotropin sekresyonu üzerindeki androjen reseptör aracılı negatif geri bildirimin kaybı ve bunun sonucunda gonadol testosteron üretiminin telafi edici şekilde artmasıdır (Wiki). Yine de bikalutamid, neden olduğu bu testosteron artışının etkilerini fazlasıyla bloke etmektedir (Wiki; Wiki) ve esasında testosteron seviyelerini bloke edebileceğinden daha fazla yükseltmesi de mümkün değildir (Wiki). Ayrıca, bikalutamid tek başına kullanıldığında, oluşan testosterondan vücutta estradiol sentezlenmeye devam eder ve bu sentez artar (Wiki). Bu nedenle bikalutamid, kendi başına önemli bir intrinsik hormonal aktiviteye sahip olmamasına rağmen, dolaylı olarak güçlü estrojenik etkiler (feminizasyon ve meme gelişimi dahil) yaratır; üstelik bu etki, ek estrojen kombinasyonu olmadan dahi gözlemlenebilmektedir (Wiki; Wiki; Neyman, Fuqua, & Eugster, 2019). Bu durum, bikalutamidin puberte çağındaki transfeminen kişilerde “puberte blokeri” olarak kullanımında önemli sonuçlar doğurmaktadır; çünkü bikalutamid, konvansiyonel puberte blokerleri (GnRH agonistleri) gibi gerçekten puberteyi durdurmak yerine, doz ile bağımlı olarak “erkek ergenliği”ni “kadın ergenliği”ne dönüştürme etkisi göstermektedir (Wiki; Neyman, Fuqua, & Eugster, 2019).
Bikalutamidin belirli sağlık riskleri bulunmaktaktadır ve bu durum, transfeminen HRT’sinde daha yaygın benimsenmemiş olmasının başlıca nedenlerindendir (Aly, 2020). Karaciğer toksisitesi riski (Wiki; Aly, 2020) ve akciğer toksisitesi (Wiki) bu risklere dahildir. Abnormal karaciger fonksiyon testleri (KCFT) (örn. yükselmiş karaciğer enzimleri veya yükselmiş bilirubin düzeyleri), bikalutamid monoterapisi artı tıbbi bakım gören cis erkeklerin yaklaşık %3,4’ünde, plasebo artı tıbbi bakım alan cis erkeklerin ise %1,9’unda görülmüştür (erken prostat kanseri klinik araştırma programında 3 yıllık takip sonrasında). Klinik çalışmalarda, bikalutamid tedavisi, karaciğer enzimlerinde aşırı yükselmeye ve potansiyel olarak ciddi karaciğer toksisitesine yol açabilme riski nedeniyle cis erkeklerin yaklaşık %0,3 ile %1,5’inde sonlandırılmak zorunda kalınmıştır (Wiki). Bugüne kadar, bikalutamid ile ilişkili ciddi karaciğer toksisitesi vakalarını içeren yaklaşık 10 yayınlanmış vaka raporu vardır; bunların sekizi prostat kanseri olan cis erkeklerde görülmüştür (Wiki; Table; Aly, 2020). Ayrıca, transfeminen kişilerde bikalutamid ile ilgili birkaç yayınlanmamış ciddi karaciğer toksisitesi vakası ve ölümler bildirilmiştir (Aly, 2020). Ancak bu bildirimler doğrulanmamış olup güvenirlilikleri belli değildir, buna ek olarak ABD FDA’ya bağlı FAERS veritabanında da bikalutamid kullanımıyla bağlantılı yüzlerce karaciğer komplikasyonu vakası bulunmaktadır (Wiki; FDA). Bikalutamidle anormal karaciğer fonksiyon testleri genellikle kullanıma başlandıktan sonraki ilk 3 ila 6 ay içinde ortaya çıkmaktadır (Kolvenbag & Blackledge, 1996; Casodex FDA KÜB/KT) ve bikalutamid ile ilgili bildirilen tüm karaciğer toksisitesi olgularının başlangıç süresi 6 aydan kısa olmuştur (Tablo). Bikalutamid ile karaciğer toksisitesinin, kullanılan klinik doz aralığındaki doz ile ilişkili (bağımlı) olup olmadığı bilinmemektedir (Wiki). Ayrıca, bikalutamidin karaciğer fonksiyon testlerinde anormallik (örn. %2,9’dan %11,4’e varan oranlarda), daha düşük dozlarda (10—50 mg/gün) ve cis kadınlarda dahi görülebilmektedir (de Melo Carvalho, 2022).
> Karaciğer toksisitesi riski nedeniyle, özellikle ilacın kullanımına başlandığı ilk 6 aylık süreç içerisinde düzenli karaciğer fonksiyon testleri (KCTF; ALT, AST, ALP, GGT) yapılması şiddetle tavsiye edilmektedir. Karaciğer toksisitesinin olası belirtileri arasında bulantı, kusma, karın ağrısı, yorgunluk, iştah kaybı, grip benzeri semptomlar ile koyu renkli idrar ve cilt/gözlerde sararma (sarılık) yer almaktadır.
Akciğer toksisitesi riski açısından bakıldığında ise bikalutamidin nadiren interstisyel pnömoni ile ilişkilendirildiği, bunun da ilerleyici akciğer fibrozuna neden olabileceği ve ölümcül olabileceği; ayrıca daha nadir olarak eozinofilik akciğer hastalığı (havayolu ve/veya akciğer dokusunda eozinofillerin artması ile karakterize edilen bir interstisyel pnömoni çeşidi) ile de ilişkili olduğu bildirilmiştir (Wiki; Tablo). Mevcut verilerde bikalutamid kullanımı ile ilişkili 17 interstisyel pnömoni ve 2 eozinofilik akciğer hastalığı vaka raporu bulunmaktadır; bunların tümü yine prostat kanseri olan cis erkeklerde görülmüştür (Tablo). Benzer şekilde, ABD FAERS veritabanında bikalutamidle ilişkili yüzlerce interstisyel pnömoni vakası bulunmaktadır (Wiki; FDA). Bikalutamid kullanımıyla interstisyel pnömoni riskinin yaklaşık 1/10.000 kişi olduğu tahmin edilmektedir; ancak bu rakam, yeterince bildirilmemiş vakalar nedeniyle düşük olabilir (Wiki; Ahmad & Graham, 2003). Asya kökenli kişilerde bikalutamid ve diğer NSAA’larla akciğer toksisitesi daha sık görülebilmektedir; bu popülasyonda daha yüksek insidanslar tespit edilmiştir (Mahler et al., 1996; Wu et al., 2022). Bikalutamidin akciğerdeki muhtemel değişimlerini düzenli olarak takip etmeyi sağlayacak bir laboratuvar testi bulunmamaktadır. İlgili akciğer toksisitesi işaretleri arasında nefes darlığı, öksürük ve farenjit (boğaz ağrısı şeklinde kendini gösteren yutak ve boğaz iltihabı) yer alır (Wiki).
Karaciğer ve akciğer toksisitesinden bağımsız olarak bikalutamid monoterapisinin prostat kanseri olan cis erkeklerde, prostat kanserinden bağımsız nedenlere bağlı ölüm riskini artırdığı bulunmuştur (Iversen et al., 2004; Iversen et al., 2006; Wellington & Keam, 2006; Jia & Spratt, 2022; Wiki). Bu nedenle bikalutamidin en erken evre prostat kanseri tedavisi için onay izni iptal edilmiş ve bu kullanım alanından vazgeçilmiştir (Wiki). Bikalutamid, daha ileri evre prostat kanserlerinin tedavisinde hâlâ onaylıdır ve kullanılmaktadır; çünkü daha ağır evrelerde bikalutamidin antiandrojenik faydaları, prostat kanseri dışındaki nedenlerle olabilecek ölüm riskini aşabilmektedir. Bikalutamidin cis erkeklerdeki ölüm riskini artırmasının altında yatan mekanizmalar tam olarak bilinmemektedir ve daha fazla veriye ihtiyaç duyulmaktadır (Wiki). Ayrıca bikalutamidin benzer şekilde transfeminen kişilerde ölüm riskini artırıp artırmayacağı da belirsizdir. Bikalutamidin ve risklerinin araştırıldığı ilgili çalışmalarda bu risklerin, transfeminen kişilerde de aynı şekilde artacağı şeklindeki varsayım ve genelleştirilmelerde bahsedilmesi gereken birçok husus bulunmaktadır. Mevcut çalışmalardaki kısıtlamalar göz önüne alındığında; araştırmalarda yer alan cis erkeklerin genellikle ileri yaşta ve hasta olması, bikalutamidin görece yüksek dozlarda (≥150 mg/gün) ve uzun süreli (örn. 5 yıl) kullanılması, gözlemlenen risklerin androjen eksikliğinden mi yoksa bikalutamidin kendine özgü yan etkilerinden mi kaynaklandığının henüz bilinmemesi ve bikalutamid monoterapisi alan prostat kanserli cis erkeklerde estradiol düzeylerinin yalnızca yaklaşık 30–50 pg/mL (110–184 pmol/L) olması (Wiki) dikkat edilmesi gereken önemli hususlardır. Bu estradiol düzeyleri kastratasyon düzeylerin üzerindedir ve kayda değer bir estrojenik etki için yeterlidir; ancak transfeminen kişiler için önerilen eşik değerler olan ≥50 pg/mL (≥184 pmol/L) alt sınırındadır. Sonuç olarak bikalutamidin cis erkeklerde artan ölüm riski ile ilişkili mekanizmaların belirsizliği ve transfeminen kişilerde de aynı riskin bulunmadığına dair klinik verilerinin ve araştırmaların eksikliği, bu riskin transfeminen popülasyonda da görülebileceği olasılığını gündemde tutmaktadır.
Bikalutamid, oral yoldan tablet formunda (örn. 50 ve 150 mg) alınır (Wiki). Gastrointestinal sistemde emilimin doygunluğa ulaşması nedeniyle, yaklaşık 150 mg/gün dozdan itibaren bikalutamidin oral biyoyararlanımı kademeli olarak düşmeye başlar ve 300 mg/gün üzerine çıkıldığında bikalutamidin seviyeleri daha fazla artmaz (Wiki; Grafik). Bikalutamidin yarılanma ömrü (vücuttan atılma süresi) oldukça uzundur (yaklaşık 6 ila 10 gün) (Wiki; Grafikler). Bu nedenle her gün alınması şart değildir; daha yüksek dozları orantılı bir şekilde, örneğin haftada bir veya iki defa alınması pratik açıdan mümkün olabilmektedir. Uzun yarı ömrü sebebiyle bikalutamidin kararlı duruma (vücutta emilen edilen ilaç miktarının vücuttan atılan ilaç miktarına eşit olduğu durum) tam olarak ulaşması yaklaşık 4 ila 12 haftayı bulabilmektedir (Wiki; Grafik; Wiki). Bununla birlikte, bikalutamidin alınmaya başlanıldığı ilk haftada kararlı durum konsantrasyonunun yaklaşık %50’sine, 3. ila 4. haftada ise %80–90’ına ulaşılır (Wiki; Grafik; Wiki). Arzu edilirse kararlı duruma daha hızlı erişmek amacıyla yükleme dozları (ilacın ilk bir/birkaç dozunun fazla alınması; örn. bikalutamid için, ilk 3-5 gün boyunca 150 mg/gün, ardından idame dozuna [50 mg/gün] geçiş) alınabilmektedir. İlk hayvan deneylerinde, bikalutamidin kan-beyin bariyerini geçmediği ve bu nedenle periferik seçiciliğe sahip olduğu (ve dolayısıyla beyindeki androjen reseptörlerini bloke etmediği) öne sürülmüştür (Wiki). Ancak sonrasında yapılan klinik araştırmalar, insanlarda durumun böyle olmadığını ve bikalutamidin merkezi sinir sistemi aracılı belirgin antiandrojenik etkiler gösterdiğini ortaya koymuştur (Wiki).
Bikalutamid ile ilişkili daha eski NSAA’lardan flutamid (piyasa isimleri Andraxan, Eulexin) ve nilutamid (piyasa isimleri Anandron, Nilandron), bikalutamide kıyasla çok daha yüksek risklere sahiptir ve transfeminen kişilerde kullanılmamalıdır. Nilutamid, geçmişte birkaç çalışmada transfeminen kişilerde antiandrojen olarak değerlendirilmiş olsa da, çok yüksek akciğer toksisitesi ve diğer yan etkileri nedeniyle daha fazla araştırılmamıştır (Aly, 2020; Wiki; Wiki). Flutamid de geçmişte kısıtlı bir şekilde transfeminen kişilerde kullanılmış; ancak bikalutamide kıyasla çok daha yüksek karaciğer toksisitesi riski, diğer yan etkiler ve dezavantajlar nedeniyle artık tercih edilmemelidir (Aly, 2020; Wiki). Enzalutamid (piyasa ismi Xtandi), apalutamid (piyasa ismi Erleada) ve darolutamid (piyasa ismi Nubeqa) gibi diğer daha yeni ve daha güçlü NSAAlar da çeşitli riskler barındırır ve şimdiye kadar prostat kanseri dışında çok az çalışmaya veya kullanıma konu olmuştur.
++++ güncel 01/2023, 07/2023, 01/2024, 03/2024 çalışmaları eklenecek.
| Minimum Doz ile Aylık Maliyetleri | Ortalama Doz ile Aylık Maliyetleri | Maksimum Doz ile Aylık Maliyetleri | Kutu fiyatı | |
| Spironolakton (Aldactonea) | 100 mg/gün Aylık 213 ₺ | 200 mg/gün Aylık 426 ₺ | 400 mg/gün Aylık 852 ₺ | 113,62 ₺ |
| Siproteron Asetat* (Androcurb) | 6,25 mg/2 gün Aylık 43,5 ₺ | 12,5 mg/2 gün Aylık 87 ₺ | 12,5 mg/gün Aylık 174 ₺ | 1.160,22 ₺ |
| Bikalutamid (Casodexc) | x2 50mg/hafta Aylık 196,8 ₺ | 25 mg/gün Aylık 328 ₺ | 50 mg/gün Aylık 656 ₺ | 612,40 ₺ |
*CPA
a 100 mg x 16 tablet olan versiyonu önerilmektedir, piyasada “Spylacton” isimli bir muadili de bulunmaktadır.
b 50 mg x 50 tablet olan versiyonu, tabletlerin rahatça dörde (ya da sekize) bölünebilmesi için önerilmektedir.
c 50 mg x 28 tablet olan versiyonu önerilmektedir.
androgenetik alopesi (erkek tipi kellik)
5α-Redüktaz İnhibitörleri
Testosteron, vücuttaki belirli dokular içinde DHT’ye dönüştürülür (Swerdloff et al., 2017). DHT, testosteronun androjen metabolitidir ve testosterona kıyasla birkaç kat daha yüksek aktiviteye sahiptir. Testosteronun DHT’ye dönüşümü 5α-redüktaz enzimi tarafından sağlanmaktadır. 5α-redüktazın bulunduğu ve testosteronun DHT’ye dönüştüğü dokular sınırlı olsa da bu dokular başlıca cilt, saç folikülleri ve prostat bezidir. DHT testosterondan daha güçlü olmasına rağmen, dolaşımdaki bir hormon olarak biyolojik rolünün minimal olduğu düşünülmektedir (Horton, 1992; Swerdloff et al., 2017). Bunun yerine, testosteron dolaşımdaki başlıca androjen işlevi görür ve DHT’nin rolünün esas olarak belirli dokularda testosteronun DHT’ye lokal metabolizması ve güçlendirilmesi aracılığıyla olduğu kabul edilir.
5α-redüktaz inhibitörleri (5α-Rİ’ler) finasterid (piyasa isimleri Proscar, Propecia, Finhair, Dilaprost) ve dutasterid (piyasa isimleri Avodart, Dutapros, Restad), 5α-redüktazı engelleyerek testosteronun DHT’ye dönüşümünü bloke eder, bu durum da dolaşımdaki ve doku içindeki DHT seviyelerinde belirgin düşüşler ile sonuçlanr. DHT’nin bir dolaşım hormonu olarak birincil rolünden ziyade dokularda aracılık eden temel faktör olması nedeniyle, 5α-Rİ’lerin antiandrojenik etkinliği oldukça sınırlıdır. Bu durum ayrıca 5α-Rİ’lerin cis erkeklerde iyi tolere edilmesi ve bu kişilerde belirgin bir maskülenite kaybına yol açmaması gerçeğiyle de desteklenmektedir (Hirshburg, 2016). 5α-Rİ’lerin tıbbi kullanımı esas olarak cis erkeklerde ve cis kadınlarda saç dökülmesi (androgenetik alopesi), cis kadınlarda hirsutizm (aşırı yüz/vücut kıllanması) ve cis erkeklerde prostat büyümesi tedavisiyle sınırlıdır. Kadınlarda akne tedavisinde de faydalı olabileceği öne sürülmüştür, ancak bu konuda kanıtlar çok sınırlıdır (Wiki). Spesifik hedefleri nedeniyle, 5α-Rİ’lerin transfeminen kişilerde genel bir antiandrojen olarak kullanılması mümkün değildir. Ayrıca, transfeminen kişilerin HRT’sinde testosteron üretiminin baskılanmasıyla birlikte DHT seviyeleri de testosteron seviyeleriyle paralel olarak azaldığından, cis kadın aralığındaki testosteron seviyelerine sahip transfeminen kişilerde 5α-Rİ’lerin rutin kullanımı sınırlı yarar sağlamaktadır ve gerekli görülmemektedir (Gooren et al., 2016; Irwig, 2020; Prince & Safer, 2020; Glintborg et al., 2021). Buna rağmen, 5α-Rİ’ler HRT almakta olan transfeminen kişilerde inatçı vücut kıllanması veya saç dökülmesi (androgenetik alopesi) yaşayanlar için, tıpkı cis kadınlarda olduğu gibi faydalı olabilmektedir (Barrionuevo et al., 2018; Prince & Safer, 2020). Ancak cis kadınlarda bu endikasyonlar için androjen reseptör antagonistlerinin etkililiğine dair veri ve kanıtların çok daha güçlü olduğu dikkate alınmalıdır (van Zuuren et al., 2015). Bu durum kulağa mantıklı gelmektedir çünkü androjen reseptör antagonistleri hem testosteronu hem de DHT’yi bloke ederken, 5α-Rİ’ler yalnızca testosteronun DHT’ye dönüşmesini engeller. Dolayısıyla 5α-Rİ’ler DHT’yi güçlü şekilde azaltır ve net etkileri antiandrojenik olsa da, testosteron seviyelerini düşürmez—ve hatta artırabilmektedir.
Üç farklı 5α-redüktaz alt tipi vardır. Dutasterid, üç alt tipin tamamını inhibe ederken finasterid yalnızca iki alt tipi inhibe eder. Bu nedenle dutasterid, finasteride kıyasla daha “tam” bir 5α-Rİ’dir. Dutasterid kandaki DHT seviyelerini %98’e kadar düşürebilirken, finasterid bu seviyeleri ancak yaklaşık %65–70 oranında azaltır. Dolaşımdaki DHT’nin neredeyse tamamı periferik dokularda sentezlendiğinden dolayı, bu oranlar dokulardaki DHT üretimindeki paralel azalmaları yansıtmaktadır (Horton, 1992). Bu bulgularla uyumlu olarak, dutasteridin cis erkeklerde saç dökülmesi tedavisinde finasteridden daha etkili olduğu bulunmuştur (Zhou et al., 2018; Dhurat et al., 2020; Wiki). Bu nedenlerle, hem finasterid hem de dutasterid etkili 5α-Rİ’ler olsa da, eğer bir 5α-Rİ kullanılacaksa dutasteridin tercih edilmesi önerilmektedir (Zhou et al., 2018; Dhurat et al., 2020).
Transfeminen kişilerde 5α-Rİ’lerin potansiyel olarak istenmeyen bir etkisi, testosteron üretimi tam olarak baskılanmamış kişilerde dolaşımdaki testosteron seviyelerini bir miktar yükseltebilmesidir (Leinung, Feustel, & Joseph, 2018; Aly, 2019; Traish et al., 2019; Irwig, 2020; Glintborg et al., 2021). Düşük testosteron seviyelerine (cis erkek aralığının altında) sahip testislere sahip kişilerde, DHT’nin hipofiz bezindeki gonadotropin salınımı üzerinde büyük bir negatif geri bildirim etkisi yaptığı düşünülmektedir (Traish et al., 2019). Bunun transfeminen kişilerdeki terapötik sonuçları —eğer varsa— belirsizdir.
5α-Rİ’lerin bir diğer potansiyel istenmeyen etkisi, sadece DHT üretimini değil, aynı zamanda bazı nörosteroidlerin de üretimini engellemeleridir. Nörosteroidler sinir sistemi —özellikle de beyin— üzerinde etkili olan steroidlerdir. 5α-Rİ’lerin sentezini engellediği nörosteroidlere örnek olarak, progesterondan oluşan allopregnanolon ve testosteron ile DHT’den türeyen 3α-androstanediol verilebilir. Çalışmalar, bu nörosteroidlerin ruh hali, anksiyete, stres ve diğer bilişsel/duygusal süreçler üzerinde önemli biyolojik düzenleyici rolleri olabileceğini göstermektedir (King, 2013). Muhtemelen bununla ilgili olarak, 5α-Rİ’lerin küçük bir depresyon riskine yol açabildiği öne sürülmüştür (Welk et al., 2018; Deng et al., 2020; Dyson, Cantrell, & Lund, 2020; Nguyen et al., 2020; Wiki). Finasterid için “post-finasterid sendromu” (PFS; Post-finasteride syndrome) olarak adlandırılan daha önemli ve kalıcı yan etkilere ilişkin çeşitli iddialar da bulunmaktadır (Traish, 2020). Ancak bu iddialar az sayıdaki raporlara dayanmaktadır ve oldukça tartışmalıdır (Fertig et al., 2016; Rezende, Dias, & Trüeb, 2018). Nosebo etkisinin (kişide ilacın kendisine yan etkiler getireceğine olan inanç), 5α-Rİ’lerle ilgili yan etki algısını daha da kötüleştirmesi muhtemeldir (Kuhl & Wiegratz, 2017; Maksym et al., 2019).
Klinik doz-aralığı çalışmalarında, genellikle kullanılan dozlardan daha düşük finasterid ve dutasterid dozlarının bile yüksek veya neredeyse maksimum düzeyde 5α-redüktaz inhibisyonu sağladığı bulunmuştur (Gormley et al., 1990; Vermeulen et al., 1991; Sudduth & Koronkowski, 1993; Drake et al., 1999; Roberts et al., 1999; Clark et al., 2004; Frye, 2006; Olsen et al., 2006; Harcha et al., 2014; Kuhl & Wiegratz, 2017). Örneğin finasterid ile yapılan bir çalışmada, DHT seviyelerinde 0,05 mg/gün’de %49,5; 0,2 mg/gün’de %68,6; 1 mg/gün’de %71,4; ve 5 mg/gün’de %72,2 oranında azalma gözlemlenmiştir (Drake et al., 1999). Benzer DHT düşüşleri kafa derisinde de kaydedilmiştir (Drake et al., 1999). Dutasterid ile yapılan bir çalışmada ise DHT seviyeleri 0,05 mg/gün’de %52,9; 0,5 mg/gün’de %94,7; 2,5 mg/gün’de %97,7 ve 5 mg/gün’de %98,4 oranında azalmıştır (Clark et al., 2004). Bu bulgular temelinde, 5α-Rİ’ler ilaç maliyetlerini azaltmak adına daha düşük dozlarda alınabilmektedirler. Finasterid tabletleri daha küçük dozlarda alınmak için bölünebilir, buna karşın; dutasterid yağ kapsülü olarak formüle edildiğinden bölünemez. Ancak dutasteridin yarı ömrü uzun olduğundan dolayı, günlük olarak alınan dozu azaltmak yerine, dozlar birkaç günde bir gibi daha az aralıklar ile alınabilir.
5α-redüktaz inhibitörleri, oral yoldan tablet ve kapsül şeklinde alınır. Finasteridin bileşik (majistral) topikal formları da mevcuttur (Marks et al., 2020). Bununla birlikte, bu preperatların aşırı dozladığı ve sistemik olarak oral finasterid formlarıyla eşdeğer DHT baskılamasına neden olabildiği gösterildiğinden dolayı alınırken dikkatli olunması önerilmektedir (Marks et al., 2020). Öte yandan daha düşük konsantrasyona sahip topikal finasterid formülasyonlarının daha lokal seçicilik sağlayabileceği düşünülmektedir (Marks et al., 2020).
Türkiye’de piyasada bulunan 5α-redüktaz inhibitörü muadilleri:
| İlaç | Muadili | Kutu Fiyatı |
|---|---|---|
| Dutasterid | Avodart 0,5 mg x 30 | 202,95 ₺ |
| Dutapros 0,5 mg x 30 | 202,95 ₺ | |
| Restad 0,5 mg x 30 | 202,95 ₺ | |
| Finasterid | Dilaprost 5 mg x 30 | 205,24 ₺ |
| Proscar 5 mg x 28 | 191,69 ₺ | |
| Finhair 1 mg x 28 | 1.003,41 ₺ | |
| Propecia 1 mg x 28 | 1.161,85 ₺ |
Transfeminen kişiler için mevcut 5α-redüktaz inhibitörü formları ve önerilen dozları:
| İlaç | Yol | Form | Dozaj |
|---|---|---|---|
| Dutasterid | Oral | Kapsül | 0,05–2,5 mg/gün |
| Finasterid | Oral | Tabletler | 0,05–5 mg/gün |
GnRH Agonistleri ve Antagonistleri
GnRH agonistleri ve antagonistleri (GnRHa), aynı zamanda GnRH reseptör agonistleri ve antagonistleri veya GnRH modülatörleri olarak da bilinir; antiandrojen olarak işlev görürler ve hipofiz bezinde GnRH’nin etkilerini engelleyerek LH ve FSH salgılanmasını baskılarlar. Normal koşullarda, reseptör agonistleri reseptörleri aktive ederken, reseptör antagonistleri bu aktivasyonu bloke ederek engeller. Ancak fizyolojik bir özelliğin sonucu olarak, GnRH agonistleri ve antagonistleri hipofiz bezinde aynı etkiyi gösterir. Bunun nedeni, normal fizyolojik koşullarda GnRH’nin nabızlar halinde (dürtüsel olarak) salgılanmasıyla, ve dışarıdan verilen GnRH agonistleriyle reseptörün kesintisiz (sürekli) şekilde uyarılmasının (egzogen GnRH agonistleriyle sürekli ve anormal şekilde reseptör aktive edildiğinde), hipofiz bezindeki GnRH reseptörünün güçlü bir şekilde duyarsızlaşarak devre dışı kalmasına yol açmasıdır (hipofiz bezindeki GnRH reseptörü desensitize olup işlevsiz hale gelir).
Sonuç olarak, hem GnRH agonistleri hem de antagonistleri gonadal cinsiyet hormonlarının üretimininin tamamen durmasına yol açar. Bu durum, testislere sahip kişilerde testosteron seviyelerini post-kastrasyon ya da cis kadın aralığına (ikisi de <50 ng/dL ya da <1,7 nmol/L) düşürür. GnRHa, geri dönüşümlü bir gonadektomiye benzetilebilir ve bu nedenle bazen “tıbbi kastrasyon” olarak da adlandırılır. Bir estrojenle birlikte kullanıldığında —seks hormonu eksikliğini önlemek için— GnRHa’nın bilinen herhangi bir ciddi yan etkisi veya riski yoktur. Bu nedenlerle, GnRHa transfeminen kişilerde kullanılabilecek en ideal antiandrojenlerdir.
GnRHa’lar puberte dönemindeki transfeminen bireylerde puberteyi baskılamak amacıyla yaygın olarak kullanılmaktadır (bkz. puberte çağındaki transfeminen kişiler). Ayrıca GnRHa’lara ulaşabilen ve erişebilen tüm yetişkin transfeminen kişilere de diğer tüm antiandrojenlerin yerine kullanımı önerilmektedir. Ne var ki, bu ilaçlar son derece pahalıdır (örn. yıllık maliyetleri: Türkiye’de yaklaşık 30.000–42.000 Türk lirası, ABD’de yaklaşık 10.000 ABD doları) ve sigorta genellikle yetişkin transfeminen bireyler için bu tedaviyi karşılamamaktadır (Türkiye’de GSS dahil olmak üzere; bkz. sonraki paragraf). Dolayısıyla, her ne kadar diğer antiandrojenlerden nispeten daha iyi bir testosteron baskılaması sağlasa da ve daha iyi bir yan etki profiline sahip olsa da, günümüzde yetişkin transfeminen bireylerde GnRHa kullanımı yaygın değildir. Bir istisna Birleşik Krallık’tadır; burada National Health Service (NHS), tüm yetişkin transfeminen bireyler için GnRH agonistlerini kapsamakta ve ödemektedir.
GnRHa’nın Ekonomik Boyutu ve Türkiye’de Ulaşılabilirliliği
GnRHa’lar Türkiye’de bulunmaktadır fakat 2024 Kasım’da piyasada bulunan neredeyse tüm formları TİTCK tarafından erişime kısıtlanmıştır (Liste). Bu kısıtlama nedeniyle yayınlanan listede yer alan ilaçlara sadece elektronik reçete ile ulaşılabilmektedir. Kısıtlanan GnRHa’lar arasında Decapeptyl (Triptorelin), Gonapeptyl (Triptorelin), Lucrin (Löprolid), Pergoveris (Follitropin ve Lutropin) ve Zoladex (Goserelin) bulunmaktadır. Eligard (Löprolid) ise bu kısıtlamada yayınlanan listede yer almamakta fakat kişi deneyimlerine dayanarak, eczacılar da bu ilacı kişilere ulaştırırken reçete istemektedirler, bu durum soru işaretlerine neden olmaktadır. Türkiye’de bulunan GnRHa’lar GSS tarafından karşılanmamaktadır, bu nedenle “cinsel kimlik bozukluğu, tanımlanmamış” (ICD Kodu: F64.9) tanısı almış trans bireyler ilaca ulaşabilse bile yüksek maliyetleri dolayısıyla genellikle reçete edilseler bile bu ilaçları kullanamamaktadırlar, bu durum dünyanın geri kalanında neredeyse aynıdır, bu GnRHa’lar reçete edilmek yerine nadiren de olsa bir GnRHa alternatifi olarak Casodex (Bikalutamid) reçete edilmektedir. Bu konu üzerinde de Türkiye’de yayımlanmış bir akademik makale bulunmaktadır (Karakilic Ozturan et al., 2023; Erişim linki).
Buserelin (Suprefact), histrelin (Supprelin; Vantas), löprolidin bazı muadilleri (Viadur; Lupron), nafarelin (Synarel), triptorelin’inin bazı muadilleri (Trelstar), abareliks (Plenaxis), degareliks (Firmagon), elagoliks (Orilissa) ve relugoliks (Relumina) Türkiye’de bulunmamaktadır.
GnRH agonistleri, hipofiz bezindeki GnRH reseptörlerinin desensitize olmasından önce, tedavinin başlangıcında kısa süreli bir testosteron artışına (flare) neden olur (Wiki). Testosteron seviyeleri yaklaşık 1,5 ila 2 kat artar; bu artış yaklaşık 1 hafta sürer ve sonrasında seviyeler düşmeye başlar (Wiki). Genellikle, kastrasyon ya da cis kadın aralığındaki testosteron düzeylerine de 2 ila 4 hafta içerisinde ulaşılır (Wiki). Buna karşın, GnRH antagonistleri ile tedavi başlandığında testosteron seviyelerinde başlangıçta herhangi bir artış görülmez; seviyeler hemen düşmeye başlar ve birkaç gün içinde kastrasyon düzeylerine inilir (Wiki; Grafik). Bunun sebebi, GnRH antagonistlerinin reseptörü önce aktive etmeden bloke etmesidir; dolayısıyla desensitizasyon mekanizmasına gerek kalmaz. Eğer gerekli görülür ya da istenirse, GnRH agonist tedavisinin başlangıcındaki testosteron artışı, antigonadotropin ajanlar—örneğin estrojen ve progestogenler—ya da bikalutamid gibi güçlü androgen reseptör antagonistleri kullanılarak önlenebilir veya azaltılabilir.
GnRH agonistlerinin uygulanması, kullanılan formülasyona bağlı olarak günde bir kez veya bir ila altı ayda bir subkutan (SubQ) ya da intramüsküler (IM) enjeksiyon şeklinde olmalıdır (buserelin, goserelin, leuprorelin, triptorelin). Alternatif olarak, bazı formları cerrahi olarak yılda bir kez implante edilebilmekte (histrelin, leuprorelin) ya da nazal sprey formunda günde iki ila üç kez kullanılabilmektedir (buserelin, nafarelin). İlk GnRH antagonistleri aylık intramüsküler (IM) veya subkutan (SubQ) enjeksiyon şeklinde uygulanmak üzere geliştirilmiştir (abarelix, degarelix). Daha yakın zamanlarda, elagolix ve relugolix gibi oral yoldan uygulanan GnRH antagonistleri tıbbi kullanıma sunulmuştur; bu ilaçlar tablet formunda, günde bir veya iki kez alınmaktadır.
Transfeminen Bireyler için Mevcut GnRH Agonistlerinin Formları ve Önerilen Dozları
| İlaç | Marka Adı | Uygulama Yolu | Form | Dozaj |
| Buserelin | Suprefact, diğerleri | Subkutan enjeksiyon | Çözelti | 200 μg/güna |
| İmplant | 6.3 mg/2 ay; 9.45 mg/3 ay | |||
| İntranazal | Nazal sprey | 400 μg, günde 3 kezb,c | ||
| Goserelin | Zoladex | Subkutan enjeksiyon | İmplant | 3.6 mg/ay; 10.8 mg/3 ay |
| Histrelin | Supprelin LA, Vantas | Subkutan implant | İmplant | 50 mg/yıl |
| Leuprorelin | Lupron, diğerleri | İntramüsküler enjeksiyon | Çözelti | 1 mg/gün |
| Eligard, Lupron Depot, Lucrin Depot, Lucrin, diğerleri | İntramüsküler/Subkutan enjeksiyon | Süspansiyon | 3.75–7.5 mg/ay; 11.25–22.5 mg/3 ay; 30 mg/4 ay; 45 mg/6 ay | |
| Viadur | Subkutan implant | İmplant | 65 mg/yıl | |
| Nafarelin | Synarel | İntranazal | Nazal sprey | 400–600 μg, günde 2–3 kez |
| Triptorelin | Decapeptyl, Trelstar Depot/LA | İntramüsküler enjeksiyon | Süspansiyon | 3.75 mg/ay; 11.25 mg/3 ay |
a İlk hafta 500 μg/günde 3 kez, sonrasında 200 μg/gün doz uygulanır.
b İlk hafta 800 μg/günde 3 kez, sonrasında 400 μg/gün doz uygulanır.
c 400 μg/günde 3 kez yerine 500 μg/günde 2 kez kullanım mümkündür; ancak bu, prostat kanseri olan cis erkeklerde yapılan çalışmaların gösterdiği üzere (%90[2] yerine %70[3] testosteron baskılaması sağlamaktadır) daha az etkilidir (Aly, 2018; Wiki).
| İlaç | Marka Adı | Uygulama Yolu | Form | Dozaj |
| Abarelix | Plenaxis | İntramüsküler enjeksiyon | Süspansiyon | 113 mg/ay |
| Degarelix | Firmagon | Subkutan enjeksiyon | Çözelti | 80 mg/ay a |
| Elagolix | Orilissa | Oral | Tablet | 150–200 mg, günde 1–2 kez b |
| Relugolix | Relumina | Oral | Tablet | 20–120 mg/günc |
a İlk ay 240 mg; sonrasında aylık 80 mg uygulanır.
b 150 mg/gün kullanımı, günde 2 kez 200 mg kullanımına göre daha az etkilidir (bu doz cis kadınlarda tam gonadal cinsiyet hormonu baskılanmasını sağlamaktadır) (Wiki).
c Tam gonadal cinsiyet hormonu baskılanması için 80–120 mg/gün; kısmi baskılama için 20–40 mg/gün dozları önerilmektedir (MacLean et al., 2015; DailyMed).
[1] Transfeminen bireyler için kullanılmamaktadır.
[2] yaklaşık ~50 ng/dL (1.7 nmol/L)
[3] yaklaşık ~180 ng/dL (6.2 nmol/L)
Androcur
➢ Güçlü testosteron baskılaması sağlamaktadır. ➢ Progestojenik etki gösteren bir androjen reseptör antagonistidir, antigonadotropik etkisiyle T üretimini ciddi oranda baskılamaktadır.
➢ Düşük dozlarda (≤12.5 mg/gün) güçlü progestojenik ve gonadotropin baskılayıcı etki sağlar.
➢ Avrupa’da transfeminenlere yönelik HRT’de en sık kullanılan antiandrojendir. Fransa’da risklerinden dolayı kullanımından kaçınılmıştır fakat bu karar yüksek doz ve uzun süre kullanımının ciddi risklere sebep olduğu yönünde çalışmalara dayanılmıştır, herhangi bir risk faktörü taşımayan, ≤12.5 mg/gün dozlarını kullanan <45 yaş grubu için risk faktörleri oldukça azdır.
➢ Yarı ömrü uzundur (~38 saat). Bu sebeple tabletler gün aşırı alınabilmektedir.
➢ T seviyesini estrojenle birlikte kullanıldığında cis kadın aralığına (<50 ng/dL [<1.7 nmol/L]) kadar kolayca düşürebilmektedir.
➢ Progestojenik etkilerden bazı kişilerde genel ruh halinin iyileşmesi, libido artışı ve uyku düzeninin düzenlenmesi gibi faydalı etkiler görülebilmektedir.
➢ Uzun yıllardır kullanılmaktadır, klinik çalışmalar yaygındır.
➢ Ciddi yan etkilerin uzun süreli kullanımda (örn. >5 yıl) görülme sıklığı artmaktadır. Bu sebepten dolayı uzun süreli kullanımı önerilmemektedir.
➢Nadir karaciğer toksisitesi riski ve çok nadir menenjiom riski (Özellikle >5 yıldan uzun süreli kullanımda).
➢Kilo artışı, yorgunluk, depresyon, cinsel istekte (libido) belirgin düşüş gibi yaygın yan etkiler ile hipofiz prolaktinoması gibi ciddi fakat çok nadir yan etkiler ortaya çıkabilmektedir.
➢Androcur’un progestojenik etkiler göstermesine bağlı olarak: olumsuz duygu durum değişiklikleri, pıhtı riski, koroner kalp hastalıkları riski, meme kanseri riski, prolaktinomlar gibi bazı kanser olmayan beyin tümörlerinin riski gibi risk faktörlerine sahip kişilerde bu risklerin görülme sıklığı artmaktadır.
➢Testosteron seviyelerini hızlı ve güçlü şekilde baskılamak isteyenler; progestojenik etkiler görmek isteyenler; prolaktin gibi kan tahlilleri yaptırabilenler.
Karaciğer hastalığı, geçmiş menenjiom öyküsü veya ailede daha önce menenjiom öyküsü, yüksek prolaktin riski olanlar, >50 yaş kişiler; ayrıca düşük doz progestojenli protokolü tolere edemeyenlere önerilmemektedir. Karaciğer fonksiyon testleri (ALT-AST), ile özellikle ilk bir yıl içinde düzenli prolaktin testi yapılması önerilmektedir.
Prolaktin seviyelerinin hedef aralığının çok üstünde çıkması halinde olası menenjiom ve prolaktinoma için beyin MR’ı çekilmesi önerilmektedir.
$ Piyasada Androcur ismi ile 50 mg’lik 50 adet tablet 1.160,22 ₺ fiyatına satılmaktadır. Aylık maliyetleri: günde 6,25 mg ile yaklaşık 174 ₺, 12,5 mg ile yaklaşık 348 ₺’dir.
Lorem ipsum dolor sit amet, consectetur adipiscing elit. Ut elit tellus, luctus nec ullamcorper mattis, pulvinar dapibus leo.
Lorem ipsum dolor sit amet, consectetur adipiscing elit. Ut elit tellus, luctus nec ullamcorper mattis, pulvinar dapibus leo.
